
ÌâÄ¿Áбí(°üÀ¨´ð°¸ºÍ½âÎö)
½«21.6g FeC2O4¸ô¾ø¿ÕÆø¼ÓÈÈ£¬·Ö½âµÃµ½10.8gÌúµÄÑõ»¯ÎÔòËùµÃÆøÌå²úÎïµÄ³É·Ö¼°ÎïÖʵÄÁ¿Îª
[¡¡¡¡]
| ||
| ʵÑé±àºÅ | T/¡æ | NO³õʼŨ¶È mol?L-1 |
CO³õʼŨ¶È mol?L-1 |
´ß»¯¼ÁµÄ±È±íÃæ»ý ©O?g-1 |
| ¢ñ | 280 | 1.2¡Á10-3 | 5.8¡Á10-3 | 82 |
| ¢ò | 124 | |||
| ¢ó | 350 | 124 |
| ÊÔ¼Á×éºÏÐòºÅ | ¹ÌÌåÊÔ¼Á£¨g£© | NH3Ìå»ý£¨mL£© | |
| a | 12.0g Ca£¨OH£©2£¨¹ýÁ¿£© | 10.8g NH4Cl | 2688 |
| b | 10.8g£¨NH4£©2SO4 | 2728 | |
| c | 12.0g NaOH£¨¹ýÁ¿£© | 10.8g NH4Cl | 3136 |
| d | 10.8g£¨NH4£©2SO4 | 3118 | |
| e | 12.0g CaO£¨¹ýÁ¿£© | 10.8g NH4Cl | 3506 |
| f | 10.8g£¨NH4£©2SO4 | 3584 | |

| ÊÔ¼Á×éºÏÐòºÅ | ¹ÌÌåÊÔ¼Á£¨g£© | NH3Ìå»ý£¨mL£© | |
| a | 12.0g Ca£¨OH£©2 £¨¹ýÁ¿£© | 10.8g NH4Cl | 2688 |
| b | 10.8g £¨NH4£©2SO4 | 2728 | |
| c | 12.0g NaOH £¨¹ýÁ¿£© | 10.8g NH4Cl | 3136 |
| d | 10.8g £¨NH4£©2SO4 | 3118 | |
| e | 12.0g CaO £¨¹ýÁ¿£© | 10.8g NH4Cl | 3506 |
| f | 10.8g £¨NH4£©2SO4 | 3584 | |

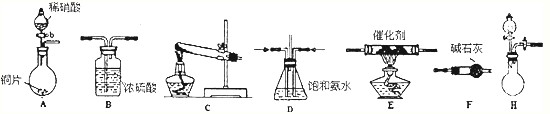
 2CO2+N2
2CO2+N2| ʵÑé±àºÅ | T/¡æ | NO³õʼŨ¶È mol?L-1 |
CO³õʼŨ¶È mol?L-1Com] |
´ß»¯¼ÁµÄ±È±íÃæ»ý ©O?g-1 |
| ¢ñ | 280 | 1.2¡Á10-3 | 5.8¡Á10-3 | 82 |
| ¢ò | 124 | |||
| ¢ó | 350 | 124 |
| ÊÔ¼Á×éºÏÐòºÅ | ¹ÌÌåÊÔ¼Á£¨g£© | NH3Ìå»ý£¨ml£© | |
| a | 12.0gCa£¨OH£©2£¨¹ýÁ¿£© | 10.8gNH4Cl | 2688 |
| b | 10.8g£¨NH4£©2SO4 | 2728 | |
| c | 12.0gNaOH£¨¹ýÁ¿£© | 10.8gNH4Cl | 3136 |
| d | 10.8g£¨NH4£©2SO4 | 3118 | |
| e | 12.0gCaO£¨¹ýÁ¿£© | 10.8gNH4Cl | 3506 |
| f | 10.8g£¨NH4£©2SO4 | 3584 | |
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com