
题目列表(包括答案和解析)
相对分子质量为204.0)测定NaOH溶液的浓度,若NaOH溶液的浓度在0.1mol•L-1左右,滴定终点时溶液的pH约为9.1。该生用托盘天平称量邻苯二甲酸氢钾时,在左盘放有一个1g砝码,游码位置如图所示:
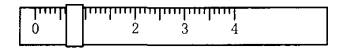
(1)将称好的邻苯二甲酸氢钾放于锥形瓶中,加适量水溶解,溶液无色,再加入指示剂________(从甲基橙、酚酞、石蕊中选择)1~2滴,用NaOH溶液滴定至终点,现象是________。
(2)该生进行三次实验,所取固体质量均相同,填写下表:
实验编号 邻苯二甲酸氢钾质
量/g 待测NaOH溶液体
积/mL
1 18.20
2 17.10
3 16.90
(3)滴定中误差较大的是第________次实验,造成这种误差的可能原因是(只填三种即可):a________b________c________
(4)NaOH溶液的物质的量浓度为(只列出计算式,不必求出结果)。
某学生用邻苯二甲酸氢钾(
相对分子质量为204.0)测定NaOH溶液的浓度,若NaOH溶液的浓度在0.1mol•L-1左右,滴定终点时溶液的pH约为9.1。该生用托盘天平称量邻苯二甲酸氢钾时,在左盘放有一个1g砝码,游码位置如图所示:
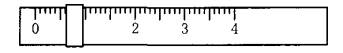
(1)将称好的邻苯二甲酸氢钾放于锥形瓶中,加适量水溶解,溶液无色,再加入指示剂________(从甲基橙、酚酞、石蕊中选择)1~2滴,用NaOH溶液滴定至终点,现象是________。
(2)该生进行三次实验,所取固体质量均相同,填写下表:
实验编号 邻苯二甲酸氢钾质
量/g 待测NaOH溶液体
积/mL
1 18.20
2 17.10
3 16.90
(3)滴定中误差较大的是第________次实验,造成这种误差的可能原因是(只填三种即可):a________b________c________
(4)NaOH溶液的物质的量浓度为(只列出计算式,不必求出结果)。
碳化硅(SiC) 、氧化铝(Al2O3) 和氮化硅(Si3N4)是优良的高温结构陶瓷,在工业生产和科技领域有重要用途。
(1)Al的原子结构示意图为 ;Al与NaOH溶液反应的离子方程式为
。
(2)氮化硅抗腐蚀能力很强,但易被氢氟酸腐蚀,氮化硅与氢氟酸反应生成四氟化硅和一种铵盐,其反应方程式为 。
(3)工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g) + 2N2(g) + 6H2(g) Si3N4(s) + 12HCl(g) △H<0
Si3N4(s) + 12HCl(g) △H<0
某温度和压强条件下,分别将0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2L密闭容器内,进行上述反应,5min达到平衡状态,所得Si3N4(s)的质量是5.60g。
①H2的平均反应速率是 mol/(L·min)。
②平衡时容器内N2的浓度是 mol·L-1。
③SiCl4(g)的转化率是 。
④若按n(SiCl4) : n(N2) : n(H2) =" 3" : 2 : 6的投料配比,向上述容器不断扩大加料,SiCl4(g)的转化率应 (填“增大”、“减”或“不变”)。
⑤工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)  Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达到平衡时,吸收热量为QkJ
C.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL1mol·L-1的NaOH恰好反应
D.反应至4min时,若HCl的浓度为0.12mol·L-1,则H2的反应速率为0.03mol/(L·min)
碳化硅(SiC) 、氧化铝(Al2O3) 和氮化硅(Si3N4)是优良的高温结构陶瓷,在工业生产和科技领域有重要用途。
(1)Al的原子结构示意图为 ;Al与NaOH溶液反应的离子方程式为
。
(2)氮化硅抗腐蚀能力很强,但易被氢氟酸腐蚀,氮化硅与氢氟酸反应生成四氟化硅和一种铵盐,其反应方程式为 。
(3)工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g) + 2N2(g) + 6H2(g) Si3N4(s) +
12HCl(g) △H<0
Si3N4(s) +
12HCl(g) △H<0
某温度和压强条件下,分别将0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2L密闭容器内,进行上述反应,5min达到平衡状态,所得Si3N4(s)的质量是5.60g。
①H2的平均反应速率是 mol/(L·min)。
②平衡时容器内N2的浓度是 mol·L-1。
③SiCl4(g)的转化率是 。
④若按n(SiCl4) : n(N2) : n(H2) =" 3" : 2 : 6的投料配比,向上述容器不断扩大加料,SiCl4(g)的转化率应 (填“增大”、“减”或“不变”)。
⑤工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)
 Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达到平衡时,吸收热量为QkJ
C.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL1mol·L-1的NaOH恰好反应
D.反应至4min时,若HCl的浓度为0.12mol·L-1,则H2的反应速率为0.03mol/(L·min)
 Si3N4(s) + 12HCl(g) △H<0
Si3N4(s) + 12HCl(g) △H<0  Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com