
题目列表(包括答案和解析)
下列关于固体物质:Cu、Si和Ne的说法中正确的是
A.Cu、Si和Ne三种晶体中,熔点最低的是Ne
B.晶体Mg属于金属晶体,其中Mg原子的堆积方式是面心立方最密堆积
C.1mol晶体Si中,含有4molSi—Si键
D.Si和Ne都是非金属元素,所以它们的晶体类型是相同的
【解析】Cu、Si和Ne形成的晶体分别是金属晶体、原子晶体和分子晶体,所以A是正确的。镁属于六方最密堆积,B不正确。1molSi含有4mol价电子,形成的共价键是,C不正确。Si形成的是原子晶体,Ne形成的是分子晶体,D不正确。答案选A。
A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层是最外层电子数的2倍,则关于A、B元素的判断正确的( )
A.A和B元素一定都是第2周期元素 B.A和B元素一定是同一主族元素
C.B元素可以是第2周期VIA族元素 D.可以相互化合形成化合物
【解析】考查原子核外电子的排布规律。元素原子最外层电子数是次外层电子数的3倍,则该元素是O,即A是O。B元素原子次外层是最外层电子数的2倍,则B可能是Li或Si。不论B是Li还是Si都可以与O形成氧化物Li2O或SiO2,所以正确的答案是D。
下列关于固体物质:Cu、Si和Ne的说法中正确的是
A.Cu、Si和Ne三种晶体中,熔点最低的是Ne
B.晶体Mg属于金属晶体,其中Mg原子的堆积方式是面心立方最密堆积
C.1mol晶体Si中,含有4molSi—Si键
D.Si和Ne都是非金属元素,所以它们的晶体类型是相同的
【解析】Cu、Si和Ne形成的晶体分别是金属晶体、原子晶体和分子晶体,所以A是正确的。镁属于六方最密堆积,B不正确。1molSi含有4mol价电子,形成的共价键是 ,C不正确。Si形成的是原子晶体,Ne形成的是分子晶体,D不正确。答案选A。
,C不正确。Si形成的是原子晶体,Ne形成的是分子晶体,D不正确。答案选A。
A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层是最外层电子数的2倍,则关于A、B元素的判断正确的( )
A.A和B元素一定都是第2周期元素 B.A和B元素一定是同一主族元素
C.B元素可以是第2周期VIA族元素 D.可以相互化合形成化合物
【解析】考查原子核外电子的排布规律。元素原子最外层电子数是次外层电子数的3倍,则该元素是O,即A是O。B元素原子次外层是最外层电子数的2倍,则B可能是Li或Si。不论B是Li还是Si都可以与O形成氧化物Li2O或SiO2,所以正确的答案是D。
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,VLCHCl3含有的碳原子数为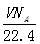
B.干冰晶胞中含有C=O键数目为4NA
C.标准状况下22.4L氩气,含氩原子的数目为2NA
D.1mol二氧化硅晶体中含有Si—O键的数目为4NA
【解析】标准状况下, CHCl3是液体,A错误。干冰晶胞中含有的CO2分子有8×1/8+6×1/2=4,但1个CO2分子中存在2个C=O,所以干冰晶胞中含有C=O键数目为8NA,B不正确。氩气是单原子分子,1mol中含有1mol氩原子,C不正确。硅原子有4个价电子,能形成4个Si—O键,D正确,答案是D。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com