
题目列表(包括答案和解析)
固体X是由两种常见元素组成的化合物,其中金属元素与另一元素的质量比为14∶1。在一定条件下X可发生如下框图的转化关系,有的反应标出全部产物,有的反应标出部分产物。已知P为两种气体的混合物,R是无色无味能使澄清石灰水变浑浊的气体,C为红褐色物质,M为常见金属单质,Q为常见非金属单质。试填空。
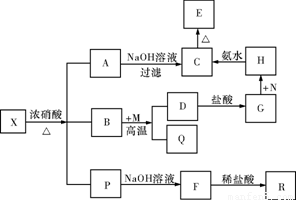
(1)X的化学式为 ,P中气体的化学式为 。
(2)实现G→H,欲不引进新的杂质,N可以选择下列物质中的 (填序号)。
①KMnO4 ②HNO3 ③H2O2 ④Cl2
(3)写出B和M反应的化学方程式: 。
(4)已知P中有一种气体与氢氧化钠溶液反应可生成两种正盐,该反应的离子方程式为 。
FeCl3溶液和Fe(OH)3胶体具有的共同性质是( )
A.都能透过滤纸 B.都呈红褐色
C.具有相同的颗粒直径 D.都存在布朗运动
FeCl3溶液和Fe(OH)3胶体具有的共同性质是( )
A.都能透过滤纸 B.都呈红褐色
C.具有相同的颗粒直径 D.都存在布朗运动
部分弱酸的电离平衡常数如下表:
|
弱酸 |
HCOOH |
HClO |
H2CO3 |
H2SO3 |
|
电离平衡常数 (25℃) |
|
|
|
|
(1)在温度相同时,各弱酸的Ki值与酸性的相对强弱的关系为:________________________。
(2)下列离子方程式正确的是
A.2ClO- + H2O + CO2 → 2HClO + CO32-
B.2HCOOH + CO32- → 2HCOO- + H2O + CO2↑
C.H2SO3 + 2HCOO- → 2HCOOH + SO32-
D.Cl2 + H2O+2CO32- → 2HCO3- + Cl- + ClO-
(3)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为 。
亚硒酸(H2SeO3)也是一种二元弱酸,常温下是一种无色固体,易溶于水,有较强的氧化性。
(4)往亚硒酸溶液中不断通入SO2 会产生红褐色单质,写出该反应的化学方程式: 。
(5)将亚硒酸与30%的H2O2加热可制得硒酸(H2SeO4),反应方程式如下:
H2SeO3 + H2O2 → H2SeO4+H2O,下列说法中正确的是…………………………………( )
A.H2O2既是氧化剂又是还原剂
B.H2O 既不是氧化产物又不是还原产物
C.H2SeO4既是氧化产物又是还原产物
D.氧化性:H2SeO3>H2SeO4
碲酸(H6TeO6)是一种很弱的酸, ,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:
,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:
HI+ H6TeO6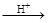 TeO2+ Te+ I2+ H2O
TeO2+ Te+ I2+ H2O
(6)若反应中生成的TeO2与Te的物质的量之比为 ,试配平上述化学方程式。
,试配平上述化学方程式。
从中选出适当的词语将其序号填入下列空格中:?
(1)在肥皂水中透过强光,可以见到光带,这种现象称为___________。?
(2)在浓肥皂水中加入饱和食盐水,肥皂凝聚,这种现象称为___________。?
(3)在Fe(OH)3溶胶中加入(NH4)2SO4溶液,产生了红褐色沉淀,这种现象叫做____________。?
(4)用半透膜把制取的Fe(OH)3溶胶中的HCl分离去的方法叫做_________。?
(5)不同牌号的蓝墨水混合后,有时会产生沉淀,这是? ?现象。?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com