
题目列表(包括答案和解析)

| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl- | 取少许滤液于试管中,加入 硝酸酸化的硝酸银溶液 硝酸酸化的硝酸银溶液 硝酸酸化的硝酸银溶液 硝酸酸化的硝酸银溶液 |
产生白色沉淀 | 含有Cl- |
| 2.检验NH4+ | 取少许滤液于试管中,加入 浓氢氧化钠溶液并加热, 浓氢氧化钠溶液并加热, 将润湿的红色石蕊试纸置于试管口附近 将润湿的红色石蕊试纸置于试管口附近 |
石蕊试纸变蓝色 石蕊试纸变蓝色 石蕊试纸变蓝色 石蕊试纸变蓝色 |
含有NH4+ k |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
| ||
| ||
| ||
| MnO2 |
| MnO2 |
A.酸性 B.氧化性 C.还原性 D.吸水性 E.脱水性 F.难挥发性
( )①Hg+2H2SO4(浓) ![]() HgSO4+SO2↑+2H2O
HgSO4+SO2↑+2H2O
( )②Cu(OH)2+H2SO4 ![]() CuSO4+2H2O
CuSO4+2H2O
( )③Fe2O3+3H2SO4 ![]() Fe2(SO4)3+3H2O
Fe2(SO4)3+3H2O
( )④2FeO+4H2SO4(浓) ![]() Fe2(SO4)3+4H2O+SO2↑
Fe2(SO4)3+4H2O+SO2↑
( )⑤2Al+3H2SO4(浓) ![]() Al2O3+3SO2↑+3H2O(Al在浓H2SO4中的变化)
Al2O3+3SO2↑+3H2O(Al在浓H2SO4中的变化)
( )⑥MnO2+4HCl![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
( )⑦2NaCl(s)+H2SO4(浓) ![]() Na2SO4+2HCl↑
Na2SO4+2HCl↑
( )⑧HCOOH浓H2SO4![]() CO↑+H2O
CO↑+H2O
( )⑨二氧化硫气体通过浓硫酸被干燥
( )⑩蘸取浓硫酸在白纸上写字,字迹变黑
( )⑾锌和稀硫酸的反应生成气体
( )⑿常温下,铁和铝在浓硫酸中“钝化”
( )⒀浓硫酸与磷酸钙混合能制得磷酸(磷酸属于弱酸)
( )⒁浓硫酸滴入浓盐酸中产生白雾
I.实验室要用98%(ρ=1.84g·cm-3)的硫酸配制3.68mol·L-1的硫酸溶液500mL
(1)需准确量取98%的硫酸 mL。
(2)准确量取一定体积的98%的硫酸后,要配制3.68mol·L-1的硫酸溶液500mL,必须用到的实验仪器是(填写序号): .
①500mL量筒 ②烧杯 ③1000mL容量瓶 ④500mL 容量瓶 ⑤天平 ⑥胶头滴管 ⑦锥形瓶 ⑧玻璃棒 ⑨酸式滴定管
(3)若配制3.68mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是 。
A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒。
B.烧杯内的稀硫酸未冷却至室温就转移至容量瓶中
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切。
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切。
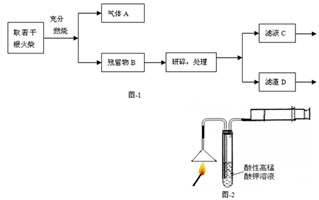
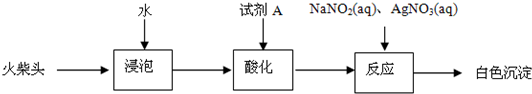
II. 某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:
普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
⑴.操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为 (填化学式);
(2)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:(答案写在答题卷上)
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl— | 取少许滤液于试管中,加入
| 产生白色沉淀 | 含有Cl— |
| 2.检验NH4+ | 取少许滤液于试管中,加入
|
| 含有NH4+ |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com