
题目列表(包括答案和解析)
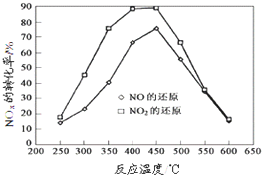 在一定条件下可用SnO2/Al2O3等多种催化剂实现丙烯选择性还原NOx,
在一定条件下可用SnO2/Al2O3等多种催化剂实现丙烯选择性还原NOx,(1)500 ℃时,将a mol SO2与b mol O2以3∶2通入固定容积为5 L的密闭容器中,
①反应进行至10 min时,测得n(SO2)=8 mol,n(SO3)=4 mol,则b=____________ mol。
②10 min内平均速率v(SO2)=___________。
③反应达平衡后,测得容器内压强是反应起始压强的0.715倍,则平衡时SO2的转化率为α1=___________。
(2)当反应温度、起始SO2与O2物质的量均与(1)相同时,将其混合气通入一恒压反应容器中,达平衡时SO2的转化率α2与(1)中转化率α1的关系是α2__________α1(填“=”“>”或“<”)。
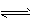 2SO3(g);正反应放热。
2SO3(g);正反应放热。 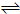 xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.
xC(g)达到平衡时,C的体积分数为W%,生成C为amol.当再投1mol A和1mol B重新达平衡.请用大于、小于、等于或不能确定填写在下列条件下从新达到平衡的结果.(18分)一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
根据题意完成下列各题:
⑴反应达到平衡时,平衡常数表达式K=
升高温度,K值 (填“增大”“减小”或“不变”)。
⑵5000C ,从反应开始到平衡,氢气的平均反应速率v(H2)= (用nB、 tB 表示)
⑶在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的1/2,下列有关该体系的说法正确的是
a .氢气的浓度减少
b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加
d.重新平衡时n(H2)/n(CH3OH)增大
⑷可逆反应:CO(g)+ 2H2(g) CH3OH(g)在恒容密闭容器中反应,达到平衡状态的标志是:
CH3OH(g)在恒容密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成2n molH2的同时生成n mol CH3OH
②单位时间内生成2n molH2 的同时,生成n mol CO
③用CO、H2、CH3OH 的物质的量浓度变化表示的反应速率的比为1 : 2 : 1的状态
④混合气体的密度不再改变的状态
⑤ 混合气体的平均相对分子质量不再改变的状态
⑸据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: (用化学方程式表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com