(2012?邗江区一模)铝镁合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
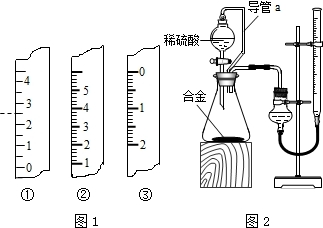
[方案一]将铝镁合金与足量NaOH溶液反应(已知2Al+2NaOH+2H
2O=2NaAlO
2+3H
2↑,而镁不与氢氧化钠溶液反应),测定剩余固体质量.
(1)称取5.4g铝镁合金粉末样品,溶于m g 质量分数为8%的NaOH溶液中.为保证合金反应完全,则NaOH溶液的体积V≧
97mL
97mL
.(假设NaOH溶液的密度为1g/mL)实验室取一定量液体一般用量筒,图1中
②
②
(填序号)是量筒的一部分,其读数为
2.6
2.6
mL.在量取液体体积时,量筒必须放平,视线要与量筒内的液体
凹液面最低处
凹液面最低处
保持水平,再读出液体体积数.
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将
偏高
偏高
(填“偏高”、“偏低”或“无影响”).
[方案二]他们设计了图2所示的实验装置.在分液漏斗中加入稀硫酸,用稀硫酸和铝镁合金反应.
(1)装置的气密性如何检查
连接好装置,从碱式滴定管加水,若滴定管中的液面和左边干燥管中的液面有稳定的高度差,则装置不漏气.
连接好装置,从碱式滴定管加水,若滴定管中的液面和左边干燥管中的液面有稳定的高度差,则装置不漏气.
;
(2)装置中导管a的作用是
保持锥形瓶和分液漏斗间的压强恒定,使稀硫酸能顺利滴下
保持锥形瓶和分液漏斗间的压强恒定,使稀硫酸能顺利滴下
和
消除因稀硫酸的滴入引起的体积误差
消除因稀硫酸的滴入引起的体积误差
.
(3)装置中有刻度的长管叫碱式滴定管,其刻度示意图如方案一第(1)题图中③所示.若实验前后碱式滴定管中液面读数分别为V
1 mL、V
2 mL.则产生氢气的体积为
V1-V2
V1-V2
mL.
(4)写出发生反应的化学方程式
Mg+H2SO4 ═MgSO4+H2↑ 2Al+3H2SO4 ═Al2(SO4)3+3H2↑
Mg+H2SO4 ═MgSO4+H2↑ 2Al+3H2SO4 ═Al2(SO4)3+3H2↑
.
[反思]:实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因
锥形瓶内生成的氢气使瓶内压强增大
锥形瓶内生成的氢气使瓶内压强增大
.
(5)若测得镁铝合金中镁的质量分数为4%,现取n克镁铝合金,投入到足量的质量分数为9.8%的稀硫酸溶液中,共收集得到氢气0.8克,则消耗的稀硫酸是
400
400
克,该合金的质量n为
7.3
7.3
.