
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
 ²»Đâ¸ÖÊÇÓÉ̀ú¡¢¸ơ¡¢Äø¡¢̀¼¼°Öڶ಻ͬԪËØËù×é³ÉµÄºÏ½đ£¬̀úÊÇÖ÷̉ª³É·ÖÔªËØ£¬¸ơÊǵÚ̉»Ö÷̉ªµÄºÏ½đÔªËØ£®
²»Đâ¸ÖÊÇÓÉ̀ú¡¢¸ơ¡¢Äø¡¢̀¼¼°Öڶ಻ͬԪËØËù×é³ÉµÄºÏ½đ£¬̀úÊÇÖ÷̉ª³É·ÖÔªËØ£¬¸ơÊǵÚ̉»Ö÷̉ªµÄºÏ½đÔªËØ£®²»Đâ¸ÖÊÇÓÉ̀ú¡¢¸ơ¡¢Äø¡¢̀¼¼°Öڶ಻ͬԪËØËù×é³ÉµÄºÏ½đ£¬̀úÊÇÖ÷̉ª³É·ÖÔªËØ£¬¸ơÊǵÚ̉»Ö÷̉ªµÄºÏ½đÔªËØ¡£ÆäÖиơµÄº¬Á¿²»ÄܵÍÓÚ11%£¬²»È»¾Í²»ÄÜÉú³ÉÖÂĂÜÑơ»¯Ä¤CrO3·ÀÖ¹¸¯Ê´¡£
(1)»ù̀¬̀¼£¨C£©Ô×ӵĹ́µÀ±íʾʽΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£
(2)[Cr(H2O)4Cl2]Cl?2H2OÖĐCrµÄÅäλÊưΪ ¡¡¡¡¡¡ £»̉ÑÖªCrO5ÖĐCrΪ+6¼Û£¬ỘCrO5µÄ½á¹¹Ê½Îª ¡¡¡¡¡¡¡¡ ¡£
(3)½đÊôÄø·ÛÔÚCOÆøÁ÷ÖĐÇá΢¼ÓÈÈ£¬Éú³ÉÎ̃É«»Ó·¢ĐỔº̀¬Ni(CO)4£¬³ÊËÄĂæ̀å¹¹ĐÍ¡£423Kʱ£¬Ni(CO)4·Ö½âΪNiºÍCO£¬´Ó¶øÖÆµĂ¸ß´¿¶ÈµÄNi·Û¡£ÊÔÍƲ⣺ËÄôÊ»ùÄøµÄ¾§̀åÀàĐÍÊÇ ¡¡¡¡ £¬ Ni(CO)4̉×ÈÜÓÚÏÂÁĐ ¡£
A£®Ë® ¡¡¡¡ B£®ËÄÂÈ»¯̀¼ ¡¡ C£®±½ ¡¡ D£®Ạ́ËáÄøÈÜ̉º
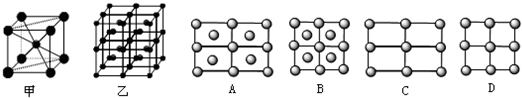
(4)FeµÄ̉»ÖÖ¾§̀åÈç¼×¡¢̉̉Ëùʾ£¬Èô°´¼×ĐéÏß·½Ị̈ÇĐ̉̉µĂµ½µÄA~BͼÖĐƠưÈ·µÄÊÇ ¡¡¡¡¡¡¡¡ ¡£


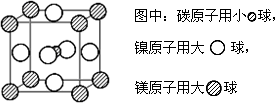
(5)¾Ư±¨µÀ£¬Ö»º¬Ă¾¡¢ÄøºÍ̀¼ÈưÖÖÔªËصľ§̀徹Ȼ¾ßÓĐ³¬µ¼ĐÔ¡£¼øÓÚƠâÈưÖÖÔªËض¼Êdz£¼ûÔªËØ£¬´Ó¶ø̉ưÆđ¹ă·º¹Ø×¢¡£¸Ă¾§̀åµÄ½á¹¹¿É¿´×÷ÓÉĂ¾Ô×ÓºÍÄøÔ×ÓÔÚ̉»Æđ½øĐĐĂæĐÄÁ¢·½Ăܶѻư£¬ÊÔĐ´³ö¸Ă¾§̀åµÄ»¯Ñ§Ê½ ¡£¾§̀åÖĐĂ¿¸öĂ¾Ô×ÓÖÜΧ¾àÀë×î½üµÄÄøÔ×ÓÓĐ ¸ö¡£
ͼÖĐ£º̀¼Ô×ÓÓĂĐ¡ |







¢ñ¡¢
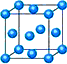
ÂÈ»¯¸ơơ£(CrO2Cl2)ÔÚÓĐ»úºÏ³ÉÖĐ¿É×÷(1)Đ´³ö¸ơÔ×ӵĻù̀¬µç×ÓÅŲ¼Ê½________£¬Óë¸ơͬÖÜÆÚµÄËùÓĐÔªËصĻù̀¬Ô×ÓÖĐ×îÍâ²ăµç×ÓÊưÓë¸ơÔ×ÓÏàͬµÄÔªËØÓĐ________(̀îÔªËØ·ûºÅ)£¬ÆäÖĐ̉»ÖÖ½đÊôµÄ¾§°û½á¹¹ÈçÏÂͼËùʾ£¬¸Ă¾§°ûÖĐº¬ÓĐ½đÊôÔ×ÓµÄÊưĿΪ________£®
(2)CrO2Cl2³£ÎÂÏÂΪÉîº́É«̉º̀壬ÄÜÓëCCl4¡¢CS2µÈ»¥ÈÜ£¬¾Ư´Ë¿ÉÅжÏCrO2Cl2ÊÇ________(̀î¡°¼«ĐÔ¡±»̣¡°·Ç¼«ĐÔ¡±)·Ö×Ó£®
(3)ÔÚ¢Ù±½
¢ÚCH3OH
¢ÛHCHO
¢ÜCS2
¢ƯCCl4
¢̃CH3Cl
¢ßHCOOHÆßÖÖÓĐ»úÎïÖÊÖĐ£¬̀¼Ô×Ó²ÉÈ¡sp2ÔÓ»¯µÄ·Ö×ÓÓĐ________(̀îĐ̣ºÅ)£¬CS2![]() ·Ö×ӵĿƠ¼ä¹¹ĐÍÊÇ________£®
·Ö×ӵĿƠ¼ä¹¹ĐÍÊÇ________£®
¢̣¡¢²»Đâ¸ÖÊÇÓÉ̀ú¡¢¸ơ¡¢Äø¡¢̀¼¼°Öڶ಻ͬԪËØËù×é![]() ³ÉµÄºÏ½đ£®
³ÉµÄºÏ½đ£®
(1)»ù![]() ̀¬̀¼(C)Ô×ӵļ۵ç×ÓÅŲ¼Ê½Îª________£®
̀¬̀¼(C)Ô×ӵļ۵ç×ÓÅŲ¼Ê½Îª________£®
(2)[Cr(H2O)4Cl2]Cl¡¤2H2OÖĐCr3+µÄÅäλÊưΪ________£»[Cr(H2O)4Cl2]ClÖĐº¬ÓеĻ¯Ñ§¼üΪ________£®
(3)½đÊôÄø·ÛÔÚCOÆøÁ÷ÖĐÇá΢¼ÓÈÈ£¬Éú³ÉÎ̃É«»Ó·¢ĐỔº̀¬Ni(CO)4£¬³ÊËÄĂæ̀å¹¹ĐÍ£®423 Kʱ£¬Ni(CO)4·Ö½âΪNiºÍCO£¬´Ó¶øÖÆµĂ¸ß´¿¶ÈµÄNi·Û£®ÊÔÍƲ⣺ËÄôÊ»ùÄøµÄ¾§̀åÀàĐÍÊÇ________£¬Ni(CO)4̉×ÈÜÓÚ________(̀îĐ̣ºÅ)£®
A£®Ë®
B£®ËÄÂÈ»¯̀¼
C£®±½
D£®Ạ́ËáÄøÈÜ̉º
(4)¾Ư±¨µÀ£¬Ö»º¬Ă¾¡¢ÄøºÍ̀¼Èư![]() ÖÖÔªËصľ§̀徹Ȼ¾ßÓĐ³¬µ¼ĐÔ£®¼øÓÚƠâÈưÖÖÔªËض¼Êdz£¼ûÔªËØ£¬´Ó¶ø̉ưÆđ¹ă·º¹Ø×¢£®¸Ă¾§̀åµÄ½á¹¹¿É¿´×÷ÓÉĂ¾Ô×ÓºÍÄøÔ×ÓÔÚ̉»Æđ½øĐĐĂæĐÄÁ¢·½Ăܶѻư£¬ÊÔĐ´³ö¸Ă¾§̀åµÄ»¯Ñ§Ê½________£®¾§̀åÖĐ
ÖÖÔªËصľ§̀徹Ȼ¾ßÓĐ³¬µ¼ĐÔ£®¼øÓÚƠâÈưÖÖÔªËض¼Êdz£¼ûÔªËØ£¬´Ó¶ø̉ưÆđ¹ă·º¹Ø×¢£®¸Ă¾§̀åµÄ½á¹¹¿É¿´×÷ÓÉĂ¾Ô×ÓºÍÄøÔ×ÓÔÚ̉»Æđ½øĐĐĂæĐÄÁ¢·½Ăܶѻư£¬ÊÔĐ´³ö¸Ă¾§̀åµÄ»¯Ñ§Ê½________£®¾§̀åÖĐ![]() Ă¿¸öĂ¾Ô×ÓÖÜΧ¾àÀë×î½üµÄÄøÔ×ÓÓĐ________¸ö£®
Ă¿¸öĂ¾Ô×ÓÖÜΧ¾àÀë×î½üµÄÄøÔ×ÓÓĐ________¸ö£®
 Ñơ»¯¼Á»̣ÂÈ»¯¼Á£¬ÄÜÓëĐí¶àÓĐ»úÎï·´Ó¦¡£Çë»Ø´đÏÂÁĐÎỀ⣺
Ñơ»¯¼Á»̣ÂÈ»¯¼Á£¬ÄÜÓëĐí¶àÓĐ»úÎï·´Ó¦¡£Çë»Ø´đÏÂÁĐÎỀ⣺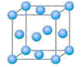
 ·Ö×ӵĿƠ¼ä¹¹ĐÍÊÇ_______¡£
·Ö×ӵĿƠ¼ä¹¹ĐÍÊÇ_______¡£ ³ÉµÄºÏ½đ¡£
³ÉµÄºÏ½đ¡£ ̀¬̀¼£¨C£©Ô×ӵļ۵ç×ÓÅŲ¼Ê½Îª¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£
̀¬̀¼£¨C£©Ô×ӵļ۵ç×ÓÅŲ¼Ê½Îª¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£ )4·Ö½âΪNiºÍCO£¬´Ó¶øÖÆµĂ¸ß´¿¶ÈµÄNi·Û¡£ÊÔÍƲ⣺ËÄôÊ»ùÄøµÄ¾§̀åÀàĐÍÊÇ ¡¡¡¡ £¬ Ni(CO)4̉×ÈÜÓÚ £῭îĐ̣ºÅ£©¡£
)4·Ö½âΪNiºÍCO£¬´Ó¶øÖÆµĂ¸ß´¿¶ÈµÄNi·Û¡£ÊÔÍƲ⣺ËÄôÊ»ùÄøµÄ¾§̀åÀàĐÍÊÇ ¡¡¡¡ £¬ Ni(CO)4̉×ÈÜÓÚ £῭îĐ̣ºÅ£©¡£ ÖÖÔªËصľ§̀徹Ȼ¾ßÓĐ³¬µ¼ĐÔ¡£¼øÓÚƠâÈưÖÖÔªËض¼Êdz£¼ûÔªËØ£¬´Ó¶ø̉ưÆđ¹ă·º¹Ø×¢¡£¸Ă¾§̀åµÄ½á¹¹¿É¿´×÷ÓÉĂ¾Ô×ÓºÍÄøÔ×ÓÔÚ̉»Æđ½øĐĐĂæĐÄÁ¢·½Ăܶѻư£¬ÊÔĐ´³ö¸Ă¾§̀åµÄ»¯Ñ§Ê½ ¡£¾§̀åÖĐ
ÖÖÔªËصľ§̀徹Ȼ¾ßÓĐ³¬µ¼ĐÔ¡£¼øÓÚƠâÈưÖÖÔªËض¼Êdz£¼ûÔªËØ£¬´Ó¶ø̉ưÆđ¹ă·º¹Ø×¢¡£¸Ă¾§̀åµÄ½á¹¹¿É¿´×÷ÓÉĂ¾Ô×ÓºÍÄøÔ×ÓÔÚ̉»Æđ½øĐĐĂæĐÄÁ¢·½Ăܶѻư£¬ÊÔĐ´³ö¸Ă¾§̀åµÄ»¯Ñ§Ê½ ¡£¾§̀åÖĐ Ă¿¸öĂ¾Ô×ÓÖÜΧ¾àÀë×î½üµÄÄøÔ×ÓÓĐ ¸ö¡£
Ă¿¸öĂ¾Ô×ÓÖÜΧ¾àÀë×î½üµÄÄøÔ×ÓÓĐ ¸ö¡£
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com