|
醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐.(已知:25℃,Ka(CH3COOH)=1.69×10-5).请回答:
|
(1) |
|
写出醋酸钠在水中发生水解反应的离子方程式:________;
|
|
(2) |
|
在CH3COONa溶液中离子浓度由大到小的顺序为________(用“ c(Bn+)”表示相应离子浓度);
|
|
(3) |
|
25℃时,醋酸的电离平衡常数表达式Ka=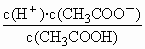 .0.10 mol/L的醋酸溶液的pH约为________(提示:醋酸的电离常数很小,平衡时的 .0.10 mol/L的醋酸溶液的pH约为________(提示:醋酸的电离常数很小,平衡时的 c(CH3COOH)可近似视为仍等于0.10 mol/L;已知:lg1.3=0.114);
|
|
(4) |
|
对于醋酸溶液和醋酸钠溶液的下列说法正确的是________;
|
| [ ] |
A. |
稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸的水解程度减小.
|
B. |
升高温度可以促进醋酸电离,而升高温度则会抑制醋酸钠水解.
|
C. |
醋酸和醋酸钠的混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离.
|
D. |
醋酸和醋酸钠的混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离.
|
|
(5) |
|
物质的量浓度均为0.1 mol/L的CH3COONa和CH3COOH溶液等体积混合(注:混合前后溶液体积变化忽略不计),混合液中的下列关系式正确的是________;
|
A. |
c (CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
|
B. |
c (Na+)+c(H+)=c(CH3COO-)+c(OH-)
|
C. |
c (CH3COO-)+c(CH3COOH)=0.1 mol/L
|
|
(6) |
|
常温时,有以下3种溶液,其中pH最小的是________
|
| [ ] |
A. |
0.02 mol·L-1CH3COOH与0.02 mol·L-1 NaOH溶液等体积混合液
|
B. |
0.03 mol·L-1 CH3COOH与0.01 mol·L-1NaOH溶液等体积混合液
|
C. |
pH=2的CH3COOH与pH=12的NaOH溶液等体积混合液
|
|
(7) |
|
已知醋酸能够和小苏打溶液发生下列反应:
CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O.用pH试纸在常温下分别测定0.10 mol/L的醋酸钠溶液和0.10 mol/L的碳酸氢钠溶液,则pH(CH3COONa)________pH(NaHCO3).(填:“>”、“<”或“=”)
|
|
