
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)

(1)ДжбЮжаКЌгаCa2+ЁЂMg2+ЁЂ![]() ЕШдгжЪРызгЃЌОЋжЦЪБЫљгУЪдМСЮЊЃКA.бЮЫсЃЛB.BaCl2ШмвКЃЛC.NaOHШмвКЃЛD.Na2CO3ШмвКЁЃдђМгШыЪдМСЕФЫГађЪЧ_________________ЁЃ(ЬюађКХ)
ЕШдгжЪРызгЃЌОЋжЦЪБЫљгУЪдМСЮЊЃКA.бЮЫсЃЛB.BaCl2ШмвКЃЛC.NaOHШмвКЃЛD.Na2CO3ШмвКЁЃдђМгШыЪдМСЕФЫГађЪЧ_________________ЁЃ(ЬюађКХ)
(2)аДГігУКЃЬВЩЯЕФБДПЧжЦCa(OH)2ЕФЛЏбЇЗНГЬЪНЃК__________________,_________________ЁЃ
(3)ЕчНтЮоЫЎMgCl2ПЩжЦШЁУОКЭCl2ЃЌЦфжаИБВњЦЗCl2КЭЗлФЉзДЪьЪЏЛвПЩжЦЕУЦЏАзЗлЁЃжЦЦЏАзЗлЕФЛЏбЇЗНГЬЪНЮЊ______________________________________________________________ЁЃ
(4)гУКЃЬВЩЯЕФБДПЧжЦCa(OH)2ЃЌЖјВЛДгвьЕиЩНжаПЊдфЪЏЛвЪЏжЦШЁЃЌжївЊПМТЧЕНЪВУДЮЪЬтЃП_______________________________________ЁЃ
(5)ДгОМУаЇвцНЧЖШПДЃЌИУЛЏЙЄГЇГЇжЗгІбЁдк___________________________ЁЃ

ЪдЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉДжбЮжаКЌгаCa2+ЁЂMg2+ЁЂ![]() ЕШдгжЪРызгЃЌОЋжЦЪБЫљгУЪдМСЮЊЃКA.бЮЫс B.BaCl2ШмвК C.NaOHШмвК D.Na2CO3ШмвКЁЃдђМгШыЪдМСЕФЫГађЪЧ____________________________ЁЃ
ЕШдгжЪРызгЃЌОЋжЦЪБЫљгУЪдМСЮЊЃКA.бЮЫс B.BaCl2ШмвК C.NaOHШмвК D.Na2CO3ШмвКЁЃдђМгШыЪдМСЕФЫГађЪЧ____________________________ЁЃ
ЃЈ2ЃЉаДГіЕчНтБЅКЭЪГбЮЫЎЕФЛЏбЇЗДгІЗНГЬЪНЁЃ
ЃЈ3ЃЉаДГігУКЃЬВЩЯБДПЧжЦCaЃЈOHЃЉ2ЕФЛЏбЇЗДгІЗНГЬЪНЁЃ
ЃЈ4ЃЉгЩMgCl2ЁЄ6H2OЭбЫЎжЦЮоЫЎMgCl2гУгкЕчНтЃЌMgCl2ЁЄ6H2OОЇЬхдк________ЦјЬхжаМгШШЭбЫЎЃЌЩњВњжаЭЈШыДЫжжЦјЬхЕФзїгУЪЧ______________________________________________ЁЃ
ЃЈ5ЃЉЕчНтЮоЫЎMgCl2ПЩжЦШЁН№ЪєУОКЭТШЦјЃЌЦфжаИБВњЦЗТШЦјКЭЗлФЉзДЪьЪЏЛвЗДгІПЩжЦЕУЦЏАзЗлЁЃжЦЦЏАзЗлЕФЛЏбЇЗДгІЗНГЬЪНЮЊ_______________________________________________ЁЃ
 КЃЫЎжаПЩЬсШЁЖржжЛЏЙЄдСЯЃЌЯТУцЪЧЙЄвЕЩЯЖдКЃЫЎЕФМИЯюзлКЯРћгУЪОвтЭМЃЎ
КЃЫЎжаПЩЬсШЁЖржжЛЏЙЄдСЯЃЌЯТУцЪЧЙЄвЕЩЯЖдКЃЫЎЕФМИЯюзлКЯРћгУЪОвтЭМЃЎ

КЃЫЎжаПЩЬсШЁЖржжЛЏЙЄдСЯЃЌЯТУцЪЧЙЄвЕЩЯЖдКЃЫЎЕФМИЯюзлКЯРћгУЪОвтЭМЁЃ
АДвЊЧѓЛиД№ЮЪЬтЃК
ЃЈ1ЃЉКЦхЋЕФКЃбѓЪЧвЛИіОоДѓЕФБІПтЃЌдЬКЌга80ЖржждЊЫиЃЌПЩЙЉЬсШЁРћгУЕФга50ЖржжЁЃЯТСаЮяжЪВЛашвЊЭЈЙ§ЛЏбЇБфЛЏОЭФмЙЛДгКЃЫЎжаЛёЕУЕФЪЧ ЁЃ
AЃЎЪГбЮ BЃЎН№ЪєФЦ CЃЎЕЫЎ
ЃЈ2ЃЉвдЕчНтЪГбЮЫЎЮЊЛљДЁжЦШЁCl2ЁЂ ЕШВњЦЗЕФЙЄвЕГЦЮЊЁАТШМюЙЄвЕЁБЁЃ
ЃЈ3ЃЉЪЕбщЪвжЦШЁТШЦјЕФЗДгІдРэЮЊЃКMnO2+4HCl(ХЈ) MnCl2+Cl2Ёќ+2H2OЃЛИљОнЩЯЪіЪЕбщдРэЃЌДгЯТСазАжУжабЁдёКЯЪЪЕФЗЂЩњзАжУгУгкЪЕбщЪвжЦШЁЩйСПТШЦј
MnCl2+Cl2Ёќ+2H2OЃЛИљОнЩЯЪіЪЕбщдРэЃЌДгЯТСазАжУжабЁдёКЯЪЪЕФЗЂЩњзАжУгУгкЪЕбщЪвжЦШЁЩйСПТШЦј
(ЬюаДзАжУЕФађКХ)ЁЃ
ЃЈ4ЃЉЪЕбщЪвжаФЃФтBrЁЊЁњBr2ЕФзЊЛЏЃЌПЩвдЭЈЙ§дкKBrШмвКжаЕЮМгЩйСПаТжЦТШЫЎЕФЪЕбщНјааЪЕЯжЁЃаДГіBrЁЊЁњBr2ЕФзЊЛЏРызгЗНГЬЪНЮЊЃК ЃЛТШЫЎВЛЮШЖЈЃЌвЊЯжгУЯжХфЃЌЯТСаЮќЪеТШЦјжЦБИТШЫЎЕФзАжУзюКЯРэЕФЪЧ ЃЈбЁЬюЯТСабЁЯюЕФБрКХзжФИЃЉЁЃ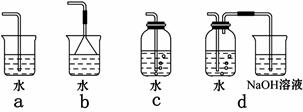
ЃЈ5ЃЉЕчНтШлШкТШЛЏУОЫљЕУЕФУОеєЦјРфШДКѓМДЮЊЙЬЬхУОЁЃЯТСаЦјЬхжаЃЌУОеєЦјПЩвддкЦфЗеЮЇжаРфШДЕФЪЧЁЁ ЁЁЃЈбЁЬюЯТСабЁЯюЕФБрКХзжФИЃЉЁЃ
AЃЎCl2ЁЁЁЁЁЁЁЁBЃЎN2ЁЁЁЁЁЁЁЁCЃЎArЁЁЁЁЁЁЁЁDЃЎПеЦјЁЁЁЁЁЁЁЁEЃЎH2
КЃЫЎжаПЩЬсШЁЖржжЛЏЙЄдСЯЃЌЯТУцЪЧЙЄвЕЩЯЖдКЃЫЎЕФМИЯюзлКЯРћгУЪОвтЭМЁЃ
АДвЊЧѓЛиД№ЮЪЬтЃК
ЃЈ1ЃЉКЦхЋЕФКЃбѓЪЧвЛИіОоДѓЕФБІПтЃЌдЬКЌга80ЖржждЊЫиЃЌПЩЙЉЬсШЁРћгУЕФга50ЖржжЁЃЯТСаЮяжЪВЛашвЊЭЈЙ§ЛЏбЇБфЛЏОЭФмЙЛДгКЃЫЎжаЛёЕУЕФЪЧ ЁЃ
AЃЎЪГбЮ BЃЎН№ЪєФЦ CЃЎЕЫЎ
ЃЈ2ЃЉвдЕчНтЪГбЮЫЎЮЊЛљДЁжЦШЁCl2ЁЂ ЕШВњЦЗЕФЙЄвЕГЦЮЊЁАТШМюЙЄвЕЁБЁЃ
ЃЈ3ЃЉЪЕбщЪвжЦШЁТШЦјЕФЗДгІдРэЮЊЃКMnO2+4HCl(ХЈ) MnCl2+Cl2Ёќ+2H2OЃЛИљОнЩЯЪіЪЕбщдРэЃЌДгЯТСазАжУжабЁдёКЯЪЪЕФЗЂЩњзАжУгУгкЪЕбщЪвжЦШЁЩйСПТШЦј (ЬюаДзАжУЕФађКХ)ЁЃ
MnCl2+Cl2Ёќ+2H2OЃЛИљОнЩЯЪіЪЕбщдРэЃЌДгЯТСазАжУжабЁдёКЯЪЪЕФЗЂЩњзАжУгУгкЪЕбщЪвжЦШЁЩйСПТШЦј (ЬюаДзАжУЕФађКХ)ЁЃ
ЃЈ4ЃЉЪЕбщЪвжаФЃФтBrЁЊЁњBr2ЕФзЊЛЏЃЌПЩвдЭЈЙ§дкKBrШмвКжаЕЮМгЩйСПаТжЦТШЫЎЕФЪЕбщНјааЪЕЯжЁЃаДГіBrЁЊЁњBr2ЕФзЊЛЏРызгЗНГЬЪНЮЊЃК ЃЛТШЫЎВЛЮШЖЈЃЌвЊЯжгУЯжХфЃЌЯТСаЮќЪеТШЦјжЦБИТШЫЎЕФзАжУзюКЯРэЕФЪЧ ЃЈбЁЬюЯТСабЁЯюЕФБрКХзжФИЃЉЁЃ
ЃЈ5ЃЉЕчНтШлШкТШЛЏУОЫљЕУЕФУОеєЦјРфШДКѓМДЮЊЙЬЬхУОЁЃЯТСаЦјЬхжаЃЌУОеєЦјПЩвддкЦфЗеЮЇжаРфШДЕФЪЧЁЁ ЁЁЃЈбЁЬюЯТСабЁЯюЕФБрКХзжФИЃЉЁЃ
AЃЎCl2ЁЁЁЁЁЁЁЁBЃЎN2ЁЁЁЁЁЁЁЁCЃЎArЁЁЁЁЁЁЁЁDЃЎПеЦјЁЁЁЁЁЁЁЁEЃЎH2
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com