食盐是日常生活的必需品,也是重要的化工原料.
(1)粗食盐常含有少量Ca
2+、Mg
2+、SO
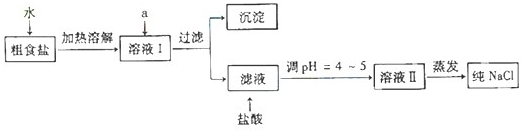
42-等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和Na
2CO
3溶液 饱和K
2CO
3溶液 NaOH溶液 BaCl
2溶液 Ba(NO
3)
2溶液
①欲除去溶液Ⅰ中的Ca
2+、Mg
2+、SO
42-离子,选出a所代表的试剂,按滴加顺序依次为
BaCl2、NaOH、Na2CO3
BaCl2、NaOH、Na2CO3
(只填化学式).
②过滤之前,怎样检验SO
42-已除去:
取少量待测液于试管中,向其中滴加氯化钡溶液,看是否有沉淀生成,若没有沉淀,则硫酸根离子已沉淀完全
取少量待测液于试管中,向其中滴加氯化钡溶液,看是否有沉淀生成,若没有沉淀,则硫酸根离子已沉淀完全
.
③过滤所需要的玻璃仪器有
漏斗、烧杯、玻璃棒
漏斗、烧杯、玻璃棒
.
④若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
生成的Mg(OH)2、CaCO3、BaCO3会与盐酸反应,从而影响制的食盐的纯度
生成的Mg(OH)2、CaCO3、BaCO3会与盐酸反应,从而影响制的食盐的纯度
.
(2)用提纯的NaCl配制250mL 2.00mol?L
-1NaCl溶液.
①所用仪器除药匙及上面过滤涉及到的外,还有
250ml容量瓶、托盘天平、胶头滴管
250ml容量瓶、托盘天平、胶头滴管
(填仪器名称).
②计算后,需称出NaOH质量为
29.3
29.3
g.
③下列操作的正确顺序是(用字母表示)
B→E→F→C→D→A→G
B→E→F→C→D→A→G
.
A.摇匀 B.称量 C.洗涤 D.定容 E.溶解 F.移液 G.装瓶
④下列操作对所得溶液浓度有何影响,在横线上填写“偏高”“偏低”或“无影响”.
A 定容时仰视容量瓶刻度线:
偏低
偏低
.B 称量时砝码生锈:
偏高
偏高
.