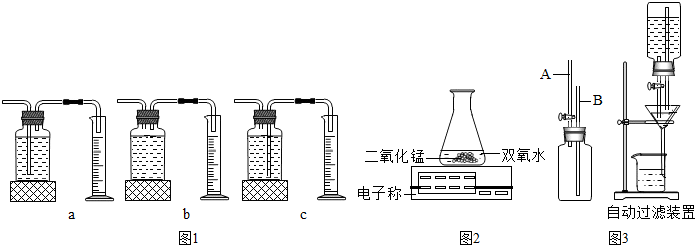
œ¬ΆΦ « Β―ι “≥Θ”ΟΒΡ Β―ι“«Τς”κΉΑ÷ΟΘ°“άΨίΧβΡΩ“Σ«σΜΊ¥πœ¬Ν–Έ ΧβΘΚ
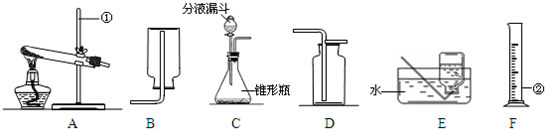
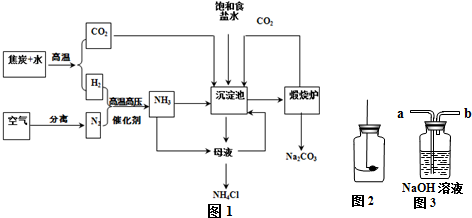
Θ®1Θ©–¥≥ω±ξΚ≈“«ΤςΒΡΟϊ≥Τ ΔΌ
ΧζΦήΧ®
ΧζΦήΧ®
ΘΜ ΔΎ
ΝΩΆ≤
ΝΩΆ≤
Θ°
Θ®2Θ© Β―ι÷Τ»Γ―θΤχ≥Θ≤…”ΟΖ÷ΫβΙΐ―θΜ·«β»ή“ΚΒΡΖΫΖ®Θ§―Γ‘ώΒΡΖΔ…ζΉΑ÷ΟΈΣ
C
C
Θ§άμ”… «
‘Ύ≥ΘΈ¬œ¬Θ§Ιΐ―θΜ·«β‘ΎΕΰ―θΜ·ΟΧΉω¥ΏΜ·ΦΝΒΡΧθΦΰœ¬ΨΆΡήΖ¥”Π
‘Ύ≥ΘΈ¬œ¬Θ§Ιΐ―θΜ·«β‘ΎΕΰ―θΜ·ΟΧΉω¥ΏΜ·ΦΝΒΡΧθΦΰœ¬ΨΆΡήΖ¥”Π
ΗΟΖΫΖ®÷Τ―θΤχ”––μΕύ”≈ΒψΘ§»γΘΚ
ΔΌΔΎ
ΔΌΔΎ
Θ®Χν–ρΚ≈Θ©Θ°
ΔΌ≤ζΈοΈόΈέ»Ψ ΔΎ≤Μ–ηΦ”»» Δέ–ηΦ”»» Δή…ζ≥…Έο÷Μ”–―θΤχ
Θ®3Θ©““Ά§―ß”Ο¥σάμ ·ΚΆœΓ―ΈΥαΖ¥”Πά¥÷Τ»ΓΕΰ―θΜ·ΧΦΘ§ΤδΖ¥”ΠΒΡΈΡΉ÷±μ¥ο ΫΈΣ
ΧΦΥαΗΤ+―ΈΥαΓ欻̷ΗΤ+Υ°+Εΰ―θΜ·ΧΦ
ΧΦΥαΗΤ+―ΈΥαΓ欻̷ΗΤ+Υ°+Εΰ―θΜ·ΧΦ
_Θ§÷Τ»Γ≤Δ ’Φ·Εΰ―θΜ·ΧΦ”ΠΖ÷±π―Γ‘ώ
CΓΔD
CΓΔD
ΉΑ÷ΟΘ®ΧνΉ÷ΡΗΘ©ΘΜ ’Φ·ΤχΧεΚσ»γΚΈΦλ―ιΦ·ΤχΤΩ÷–ΒΡΕΰ―θΜ·ΧΦ «Ζώ“―Ψ≠ ’Φ·¬ζΘΩ
ΫΪ“ΜΗυ¥χ»Φ…’ΒΡΡΨΧθΤΫΖ≈‘ΎΦ·ΤχΤΩΩΎΘ§ΡΨΧθœ®ΟπΘ§÷ΛΟς¬ζΝΥ
ΫΪ“ΜΗυ¥χ»Φ…’ΒΡΡΨΧθΤΫΖ≈‘ΎΦ·ΤχΤΩΩΎΘ§ΡΨΧθœ®ΟπΘ§÷ΛΟς¬ζΝΥ
Θ°
Θ®4Θ©Ρ≥Μ·―ß–Υ»Λ–ΓΉιΒΡΆ§―ßΘ§άϊ”Οœ¬Ν–“«ΤςΫχ–– Β―ιΘ®Υυ”–ΉΑ÷ΟΒΡΤχΟή–‘ΕΦ“―Φλ≤ιΆξ±œΘ©
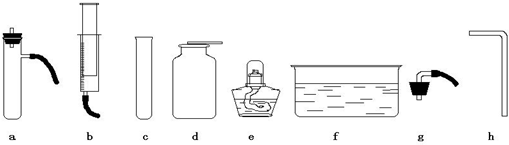
ΔΌΑ―Ιΐ―θΜ·«β»ή“ΚΜΚΜΚΦ”»κ Δ”–Εΰ―θΜ·ΟΧΒΡ»ίΤς÷–÷Τ»Γ≤Δ”Ο≈≈ΤχΖ® ’Φ·―θΤχΘ§Άξ≥…ΗΟ Β―ιΡψΥυ―Γ”ΟΒΡ“«Τς”–
abdh
abdh
Θ®ΧνΉ÷ΡΗΘ©Θ°
–¥≥ωΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖϊΚ≈±μ¥ο Ϋ
Θ°’β÷÷ΖΫΖ®”κΓΑΑ―Εΰ―θΜ·ΟΧΦ”»κ Δ”–Ιΐ―θΜ·«β»ή“ΚΒΡ ‘Ιή÷–÷Τ―θΤχΓ±œύ±»”–
Ω…“‘ΩΊ÷ΤΖ¥”ΠΒΡΫχ––Θ§ΫΎ‘Φ“©ΤΖ
Ω…“‘ΩΊ÷ΤΖ¥”ΠΒΡΫχ––Θ§ΫΎ‘Φ“©ΤΖ
ΒΡ”≈ΒψΘ°
ΔΎΡ≥Ά§―ßΦΧ–χΧΫΨΩΓΑΚλΉ©ΖέΡ© «Ζώ“≤Ω…“‘ΉςΙΐ―θΜ·«βΖ÷ΫβΖ¥”ΠΒΡ¥ΏΜ·ΦΝΘΩΓ± Β―ι≤Ϋ÷ηΚΆœ÷œσ»γœ¬ΘΚ
aΓΔΥϊΖ÷±πœρΝΫ÷ß ‘Ιή÷–Φ”»κœύΆ§ΒΡΙΐ―θΜ·«β»ή“ΚΘ§œρΤδ÷–“Μ÷ß ‘ΙήΦ”»κ“Μ“©≥ΉΚλΉ©ΖέΡ©Θ§»ΜΚσΫΪΝΫ÷ß ‘Ιή÷–ΒΡΤχΧεΒΦ≥ωΆ®»κΥ°÷–±»Ϋœ≤ζ…ζΤχ≈ίΒΡΩλ¬ΐΘ§ΖΔœ÷Φ”»κΚλΉ©ΖέΡ©ΒΡ ‘Ιή÷–Ζ¥”ΠΫœΩλΘ°
bΓΔΫΪΖ¥”ΠΫœΩλΒΡ ‘ΙήΡΎΙΧΧεΙΐ¬Υ≥ωά¥Θ§œ¥Β”ΓΔΚφΗ…ΓΔ≥ΤΝΩΘ°
cΓΔ”Ο≥ΤΝΩΚσΒΡΙΧΧε÷ΊΗ¥≤Ϋ÷ηaΒΡ Β―ιΘ§œ÷œσ”κ≤Ϋ÷ηaΆξ»ΪœύΆ§Θ°
‘ΜΊ¥πΘΚ≤Ϋ÷ηa÷–Υϊ≥ΐΝΥ―Γ”Ο ‘ΙήΆβΜΙ”ΟΒΫ…œΟφΝ–≥ωΒΡ“«Τς”–
ghf
ghf
Θ®ΧνΉ÷ΡΗΘ©Θ°≤Ϋ÷ηcΒΡ Β―ιΡΩΒΡ «
Φλ―ιΚλΉ©ΖέΒΡΜ·―ß–‘÷ ‘ΎΖ¥”Π«ΑΚσ «Ζώ”–±δΜ·
Φλ―ιΚλΉ©ΖέΒΡΜ·―ß–‘÷ ‘ΎΖ¥”Π«ΑΚσ «Ζώ”–±δΜ·
Θ°ΗΟ―ß…ζ»œΈΣΆ®Ιΐ…œ ω Β―ι“―÷ΛΟςΚλΉ©ΖέΡ©Ω…“‘ΉςΙΐ―θΜ·«βΖ÷ΫβΖ¥”ΠΒΡ¥ΏΜ·ΦΝΘ§ΒΪάœ Π»œΈΣΗΟΆ§―ßΒΡ Β―ιΜΙ»±…Ό“ΜΗωΙΊΦϋ≤Ϋ÷ηΘ§«κ÷Η≥ωά¥
Ζ¥”Π«ΑΟΜ”–≥Τ≥ωΚλΉ©ΖέΒΡ÷ ΝΩ
Ζ¥”Π«ΑΟΜ”–≥Τ≥ωΚλΉ©ΖέΒΡ÷ ΝΩ
Θ°
Θ®5Θ©‘Ύ―ßœΑ÷–Έ“Ο«ΝΥΫβΒΫ≥Θ”Ο÷Τ»Γ―θΤχΒΡΖΫΖ®”–»γΆΦΥυ ΨΒΡΥΡ÷÷ΘΚ
«κΜΊ¥πΈ ΧβΘΚ‘Ύ Β―ι “Α¥¬Χ…ΪΜ·―ßΒΡ“Σ«σΡψ»œΈΣΡ«÷÷÷Τ»Γ―θΤχΒΡΖΫΖ®ΫœΚΟΒΡ «
““
““
ΖΫΖ®Θ°Θ®ΧνΓΑΦΉΓΔ““ΓΔ±ϊΓΔΕΓΓ±Θ©–¥≥ωΦΉΖΫΖ®÷Τ»Γ―θΤχΒΡΜ·―ßΖϊΚ≈±μ¥ο Ϋ
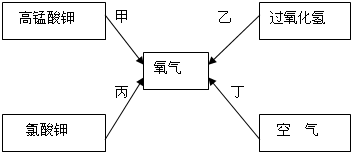






 2KCl+3O2ΓϋΘ§CuO“≤Ω…Ής¬»ΥαΦΊΖ÷ΫβΒΡ¥ΏΜ·ΦΝΘ°ΦΉΆ§―ßΈΣΧΫΨΩ¥ΏΜ·ΦΝΒΡ÷÷άύΕ‘¬»ΥαΦΊΖ÷ΫβΥΌ¬ ΒΡ”ΑœλΘ§…ηΦΤΝΥ“‘œ¬Ε‘±» ‘―ιΘΚ
2KCl+3O2ΓϋΘ§CuO“≤Ω…Ής¬»ΥαΦΊΖ÷ΫβΒΡ¥ΏΜ·ΦΝΘ°ΦΉΆ§―ßΈΣΧΫΨΩ¥ΏΜ·ΦΝΒΡ÷÷άύΕ‘¬»ΥαΦΊΖ÷ΫβΥΌ¬ ΒΡ”ΑœλΘ§…ηΦΤΝΥ“‘œ¬Ε‘±» ‘―ιΘΚ