МюЪНЬМЫсУОУмЖШаЁЃЌЪЧЯ№НКжЦЦЗЕФгХСМЬюСЯЃЎЦфзщГЩвЛАувдxMgCO
3?yMgЃЈOHЃЉ
2БэЪОЃЎ
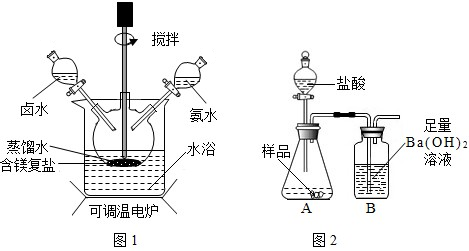
ЁОЬНОПвЛЁП
МюЪНЬМЫсУОЕФжЦБИМюЪНЬМЫсУОПЩгУMgCO
3КЭЃЈNH
4ЃЉ2CO
3зїдСЯжЦБИЃЎШЁвЛЖЈСПЕФдСЯЗХШыШ§ОБЩеЦПжаЃЌВЂНЋШ§ОБЩеЦПЗХдкКуЮТЫЎдЁЙјжаМгШШЃЈШчЭМЫљЪОЃЉЃЌМгШывЛЖЈСПеєСѓЫЎЃЌПЊЦєНСАшЦїЭЌЪБМгШыдЄЖЈЕФАБЫЎЃЌД§ЮТЖШЕНДя40ЁцЪБЕЮМгТБЫЎЃЈТШЛЏУОШмвКЃЉВЂМЬајЕЮШыАБЫЎЃЌБЃГж10ЗжжгЃЌвЛЖЮЪБМфКѓЙ§ТЫЯДЕгЃЌТЫГіЕФЙЬЬхдк120ЁцИЩдяЕУЕНМюЪНЬМЫсУОВњЦЗЃЎЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЂйНСАшЕФФПЕФЪЧ
МгПьдСЯЕФШмНтЫйЖШ
МгПьдСЯЕФШмНтЫйЖШ
ЃЛЂкбЁдёЫЎдЁМгШШЗНЪНЃЌЦфгХЕуЪЧ
ЪмШШОљдШ
ЪмШШОљдШ
ЃЎ
ЃЈ2ЃЉЫљЕУМюЪНЬМЫсУОВњЦЗжаГЃМьГігаЩйСПCl-ЃЌЦфдвђЪЧЛьга
NH4Cl
NH4Cl
ЃЈЬюЛЏбЇЪНЃЉЃЎ
ЃЈ3ЃЉЭМ1ЩшМЦЪЕбщМьбщМюЪНЬМЫсУОжаКЌгаCl-
| ЪЕ бщ Вй зї |
ЪЕбщЯжЯѓ |
ЪЕбщНсТл |
ЂйШЁбљШмНтЃЌЯђбљЦЗШмвКжаЕЮМгЙ§СПЯЁЯѕЫсЃЎ
ЂкдйЯђЩЯЪіЫљЕУШмвКМгЯѕЫсвј ЯѕЫсвј ШмвК |
ЯжЯѓЂй гаЦјХнВњЩњ гаЦјХнВњЩњ ЃЛ
ЯжЯѓЂкгаАзЩЋГСЕэЩњГЩ гаАзЩЋГСЕэЩњГЩ ЃЛ |
КЌгаCl- |
ЁОЬНОПЖўЁПЖЈСПВтЖЈМюЪНЬМЫсУОЕФзщГЩ
ЯжРћгУЭМ2ЫљЪОзАжУЃЈЭМжаМаГжвЧЦїТдШЅЃЉНјааЪЕбщЃЌГфЗжЗДгІКѓЃЌВтЖЈBжаЩњГЩЕФBaCO
3ГСЕэжЪСПЃЌвдШЗЖЈМюЪНЬМЫсУОжаMgCO
3ЕФжЪСПЗжЪ§ЃЎЧыЛиД№ЯТСаЮЪЬтЃЎ
ЃЈ1ЃЉШєВтЖЈжЕБШЪЕМЪжЕаЁЃЌПЩФмЕФдвђга
ЂкЂлЂм
ЂкЂлЂм
ЃЎЃЈЬюађКХЃЉ
ЂйзАжУAжаЫЎеєЦјЁЂHClЕШНјШызАжУBжа
ЂкзАжУAжаCO
2ЮДЭъШЋНјШызАжУB
ЂлCO
2ЦјСїЫйЖШЬЋПьЕМжТBaЃЈOHЃЉ
2ЮДЭъШЋЮќЪе
ЂмбЮЫсЮДЕЮМгЙ§СП
ЃЈ2ЃЉЮЊМѕЩйЮѓВюЃЌЯжВЩШЁвЛаЉДыЪЉЃКЮЊЗРжЙHClНјШыBзАжУЃЌПЩдкAЁЂBжЎМфдіМгзАга
ЧтбѕЛЏФЦ
ЧтбѕЛЏФЦ
ЃЈЬювЉЦЗУћГЦЛђЛЏбЇЪНЃЉШмвКЕФЯДЦјЦПЃЛНЋзАжУBжаЕФГЄЕМЙмЯТЗНдіМгвЛИіДјПзЧђХнЃЌПЩвдЬсИп
ЗДгІЫйЖШ
ЗДгІЫйЖШ
ЃЛдкзАжУBЕФКѓУцдйдіМгвЛИізАга
МюЪЏЛв
МюЪЏЛв
ЃЈЬювЉЦЗУћГЦЛђЛЏбЇЪНЃЉЕФИЩдяЙмЃЎ
ЃЈ3ЃЉзМШЗГЦШЁ8.00gбљЦЗШ§ЗнЃЌНјааВтЖЈЃЌВтЕУBaCO
3ЦНОљжЪСПЮЊ3.94gЃЎЪдМЦЫубљЦЗжаMgCO
3ЕФжЪСПЗжЪ§ЃЈаДГіМЦЫуЙ§ГЬЃЉЃЎ

