
题目列表(包括答案和解析)
实验时可供选择的试剂有:①未知浓度的NaOH溶液;②37%盐酸;③40%硫酸;④14%盐酸;⑤大理石;⑥K2CO3固体.
实验室现有如下仪器:铁架台、启普发生器、量筒、烧杯、乳胶管、玻璃导管、玻璃棒、分液漏斗.
下表所列为有关物质在常温时溶解度(g/100 g水):
|
Na2CO3 |
NaHCO3 |
NaCl |
Na2SO4 |
NaHSO4 |
NaOH |
|
15.9 |
8.40 |
35.8 |
35.5 |
20.0 |
40.0 |
(1)本实验应选用的仪器,除启普发生器、乳胶管、玻璃导管外,还应有______________.
(2)为保证制得的Na2CO3溶液尽量纯,应选用的药品除①外,还应需要_____________.
(3)简要叙述实验步骤,直到制得纯Na2CO3溶液(仪器安装不必叙述).
①量取两份相同体积的NaOH溶液;②_______________________________;③______
_______________________________.
(4)根据给出的溶解度数据,若保证在配制过程中不析出晶体,所用NaOH溶液中含有NaOH的质量分数的最大值是多少(写出计算步骤和必要的文字说明).
|
燃烧0.2 mol某有机物,得到0.4 mol CO2和0.6 mol H2O,由此可以得出的结论是 | |
| [ ] | |
A. |
该有机物含有2个碳原子和6个氢原子 |
B. |
该有机物中碳元素和氢元素的原子个数比为3∶1 |
C. |
该有机物中含有2个CO2和3个H2O |
D. |
该有机物的1个分子中含有2个碳原子和6个氢原子,还可能含有氧原子 |
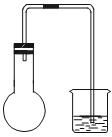
时间/h | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
A瓶(盛干燥铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
B瓶(盛醮了食盐水的铁丝) | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
C瓶(盛醮了清水的铁丝) | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
D瓶(盛完全浸没在食盐水中的铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
E瓶(盛完全浸没在清水中的铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
(1)实验开始时,要检验烧瓶的气密性,具体操作方法是_________________。
(2)该实验的目的是______________。
(3)通过本实验可以得出的结论是_______________________。
已知原子序数依次增大的A、B、C、D、E五种元素中有2种为非金属元素,其原子序数均小于30。其中A、B、C、E的价电子层中均有2个未成对电子,A、B同族且可以形成原子个数比为1:1的化合物BA,属于原子晶体。回答下列问题:
(1)在地壳中A、B元素的含量的关系为 大于 (用元素符号回答)。
(2)AO2和BO2分别为A和B的最高价氧化物,两种氧化物中含有π键的物质的电子式
为 。从原子半径大小的角度分析,A或B与氧原子形成π键难易程度的差异 。
(3)C元素在元素周期表中的位置为 ,其最高化合价为 。C单质晶体的堆积方式为 ,每个晶胞中实际占有C原子的个数为 。
(4)D与E同族且不相邻,D存在D2+和D3+两种常见离子,它们与K+及CN-能形成一种可溶性蓝色化合物,用作染料。它的结构单元如图所示,则在该晶体中n(CN-):n(K+):n(D3+):n(D2+)= ,该蓝色化合物可以由D3+与K4〔D(CN)6〕制得,也可由D2+与K3〔D(CN)6〕制得。请写出K4〔D(CN)6〕与Cl2反应生成K3〔D(CN)6〕的化学方程式 。

Ⅰ.甲、乙、丙、丁、戊具有如图所示的结构或结构单元,图中四面体外可能有的部分未画出,只有实线表示共价键,X、Y可同可不同。
已知:甲、乙晶体类型相同,单质甲能与乙发生置换反应,丙、丁、己三种粒子均含有等量的总电子数,其中丙、己是同一类晶体中的分子,己在常温下呈液态,能产生两种10电子的离子,丁是阳离子且与丙符合“等电子原理”(具有相同电子数和原子数的分子或离子互称为等电子体),戊通常为气体与丙结构相似,但分子中多了24个价电子。
(1)写出液态己产生两种等电子粒子的电离方程式: 。
(2)X、Y原子的最外层都满足8电子的分子是 (填字母代号)
A.甲 B.乙 C.丙 D.戊 E.己
(3)写出甲与乙发生置换反应的反应方程式: 。
(4)丙是目前重要的能源之一。
①丙和己在催化、加热条件下得到可燃性的两种气体,其反应的化学方程式是: 。
②现代高能电池中,常用丙作燃料电池的原料,在碱性介质(KOH溶液)的情况下,其正极反应的电极方程式为 。
(5)请写出一种与戊符合“等电子原理”的离子 。
Ⅱ.A 、B 、C 、D 、E 五种短周期元素,原子序数依次增大.A、D同主族,A 与B 、C 分别构成电子数相等的化合物w、k,且w是一种能产生温室效应的气体;D 元素最外层电子数是次外层电子数的3 倍;A 、B 、C 、D 可形成化合物x;A 、D 、E 可形成化合物y;A 、C 、D 可形成化合物z.x、y、z 均为阳离子和阴离子个数比是1 : 1 的离子化合物.回答下列问题:
(1)y的电子式为_________________;w属于______ (填“极性”或“非极性)分子;
(2)与E 同主族且为第七周期的元素原子序数为_________________;
(3)在同主族氢化物的性质递变中,k 的沸点反常,这可以用__________来解释(填字母序号);
A.共价健 B.离子键 C.氢键 D.范德瓦耳斯力
(4)常温下,x 与y以物质的量之比1 : 2 反应后所得溶液显_______(填“酸”、“碱”或“中”)性,由产物分析,原因是________________________(用离子方程式表示);
(5)由k与D 的单质、KOH 溶液构成原电池,负极会产生C 的单质。则其负极反应为______________________________;一段时间后,溶液pH__________(填“增大”、“减小”或“不变” )。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com