
题目列表(包括答案和解析)
固体单质A和气体单质B在容积一定的密闭容器中完全反应生成气体C,同温下测得容器内压强不变,且反应后气体C的密度是原气体密度的4倍。则下列判断正确的是
A.生成的气体C为单质,且B和C的摩尔质量比为1∶4
B.生成物C中A的质量分数为75%
C.生成物C中A、B的原子个数比为3∶1
D.反应前后气体分子数比为1∶4
在密闭容器中进行反应CH4(g)+H2O(g)  CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是
CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是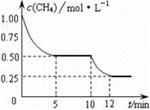
| A.0~5 min内,v(H2)=0.1 mol·(L·min)-1 |
| B.反应进行到12min时,CH4的转化率为25% |
| C.恒温下,缩小容器体积,平衡后H2浓度减小 |
| D.10 min时,改变的外界条件可能是升高温度 |
一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应: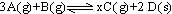 。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是
。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L。下列判断正确的是
| A.该条件下此反应的化学平衡常数约为0.91(L/mol)3 |
B.A的平均反应速率为0.3mol/(L s) s) |
| C.B的转化率为60% |
| D.若混合气体的密度不再改变时,该反应不一定达到平衡状态 |
在一定条件下,将3 molA和1 molB两种气体混合于固定容积为2 L的密闭容器中,
 发生如下反应:3A(g)+B(g)
xC(g)+2D(g) 。2 min末该反应达到平衡,生成0.8molD,
发生如下反应:3A(g)+B(g)
xC(g)+2D(g) 。2 min末该反应达到平衡,生成0.8molD,
并测得C的浓度为0.2mol·L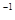 下列判断正确的是
下列判断正确的是
A.平衡常数约为0.3
B.B的转化率为60%
C.A的平均反应速率为0.3mol·(L·min)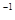
D.若混合气体的密度不变则表明该反应达到平衡状态
25℃时,在浓度均为1 mol/L 的NH4Cl、NH4HCO3、NH4HSO4溶液中,测得其中c(NH4+)分别为 a、b、c(mol/L),则下列判断正确的是
A 、a>b>c B、 c>a>b C 、b>a>c D、 a>c>b
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com