
题目列表(包括答案和解析)
石英晶体的平面示意图如下图,它实际上是立体的网状结构,其中硅、氧原子数比是m
∶n,有关叙述正确的是( )
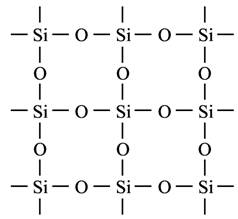
A.m∶n=1∶2
B.m∶n=2∶1
C.原硅酸根![]() 的结构为[
的结构为[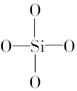 ]4-,则二聚硅酸根离子
]4-,则二聚硅酸根离子![]() 中的x=6
中的x=6
D.六聚硅酸根[Si6O19]y-中的y=10

| A.m∶n=1∶2 |
| B.m∶n=2∶1 |
C.原硅酸根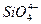 的结构为[ 的结构为[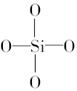 ]4-,则二聚硅酸根离子 ]4-,则二聚硅酸根离子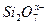 中的x=6 中的x=6 |
| D.六聚硅酸根[Si6O19]y-中的y=10 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com