
题目列表(包括答案和解析)
反应速率v和反应物浓度的关系是用实验方法测定的,化学反应H2+Cl2===2HCl的反应速率v可表示为v=k[c(H2)]m[c(Cl2)]n,式中k为常数,m、n值可用下表中数据确定之。
|
|
c(H2)(mol·L-1) |
c(Cl2)(mol·L-1) |
v(mol·L-1·s-1) |
|
① |
1.0 |
1.0 |
1.0k |
|
② |
2.0 |
1.0 |
4.0k |
|
③ |
2.0 |
4.0 |
8.0k |
由此可推得,m、n值正确的是
A、m=2,n=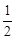 B、m=
B、m=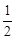 ,n=
,n=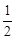 C、m=2,n=1
D、.m=1,n=
C、m=2,n=1
D、.m=1,n=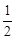
一种高分子化合物(Ⅵ)是目前市场上流行的墙面涂料之一,其合成路线如下(反应均在一定条件下进行):
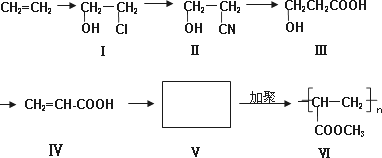
回答下列问题:
(1)化合物Ⅲ生成化合物Ⅳ的副产物为________.(提示:原子利用率100%,即原子全部都转化成产物)
(2)CH2=CH2与溴水反应方程式:________.
(3)写出合成路线中从化合物Ⅳ到化合物Ⅴ的反应方程式:________.
(4)下列关于化合物Ⅲ、Ⅳ和Ⅴ的说法中,正确的是________.
A.化合物Ⅲ可以发生氧化反应
B.化合物Ⅲ不可以与NaOH溶液反应
C.化合物Ⅳ能与氢气发生加成反应
D.化合物Ⅲ、Ⅳ和Ⅴ均可与金属钠反应生成氢气
E.化合物Ⅳ和Ⅴ均可以使溴的四氯化碳溶液褪色
F.化合物Ⅴ可以发生水解反应
反应速率v和反应物浓度的关系是用实验方法测定的,化学反应H2+Cl2===2HCl的反应速率v可表示为v=k[c(H2)]m[c(Cl2)]n,式中k为常数,m、n值可用下表中数据确定之。
|
| c(H2)(mol·L-1) | c(Cl2)(mol·L-1) | v(mol·L-1·s-1) |
| ① | 1.0 | 1.0 | 1.0k |
| ② | 2.0 | 1.0 | 4.0k |
| ③ | 2.0 | 4.0 | 8.0k |
由此可推得,m、n值正确的是
A、m=2,n= B、m=
,n=
C、m=2,n=1 D、.m=1,n=
| A、氢处于第一周期 | B、氯处于ⅦA族 | C、第三周期共有8种元素 | D、第一主族元素全部是金属 |

| ||
| ||
| 操作步骤及实验现象 | 简答 |
| ①称取3.2g氧化铁与2g炭粉均匀混合,放入48.48g的玻璃管中,按如图装置连接 | |
| ②加热前,先通一段时间纯净、干燥的氮气 | 其目的是: 排尽装置中的空气(或氧气) 排尽装置中的空气(或氧气) |
| ③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 该现象说明: 该现象说明:有CO2气体生成 该现象说明:有CO2气体生成 |
| ④完全反应后,冷却至室温,称得玻璃管和固体的总质量为52.24g |
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com