
题目列表(包括答案和解析)

实验中用到的试剂可在下列试剂中选择:
①质量分数为98%的浓H2SO4 ②质量分数为70%的硫酸 ③质量分数为25%的H2SO4 ④新开封的Na2SO3粉末 ⑤硫化亚铁(块状固体,不溶于水) ⑥NaOH溶液 ⑦溴水 ⑧Na2CO3溶液
在实验开始后不久即在B瓶中出现固体粉状物质。试完成下列问题:
(1)A中分液漏斗盛放的试剂是__________,烧瓶中盛放的试剂是__________。其实验开始时反应的化学方程式是__________________________________________________。
(2)B中反应的化学方程式是____________________,反应的氧化产物与还原产物的物质的量之比是__________。
(3)E(启普发生器)中盛放的两种试剂发生反应的化学方程式是____________________。
(4)如果A、E两装置气体生成的速度相同,流量也相同,在D中发生反应的化学方程式是______________________________。
(5)D的作用是______________________,C的作用是______________________。

实验中用到的试剂可在下列试剂中选择:
①质量分数为98%的浓H2SO4 ②质量分数为70%的硫酸③质量分数为25%的H2SO4 ④新开封的Na2SO3粉末 ⑤硫化亚铁(块状固体,不溶于水) ⑥NaOH溶液 ⑦溴水⑧Na2CO3溶液
在实验开始后不久即在B瓶中出现固体粉状物质。试完成下列问题:
(1)A中分液漏斗盛放的试剂是___________,烧瓶中盛放的试剂是___________。其实验开始时反应的化学方程式是_________________________________。
(2)B中反应的化学方程式是____________________________________________,反应的氧化产物与还原产物的物质的量之比是______________________。
(3)E(启普发生器)中盛放的两种试剂发生反应的化学方程式是______________________。
(4)如果A、E两装置气体生成的速度相同,流量也相同,在D中发生反应的化学方程式是_________________________________。
(5)D的作用是______________________,C的作用是_____________________________。

实验中用到的试剂可在下列试剂中选择:
①质量分数为98%的浓H2SO4 ②质量分数为70%的硫酸 ③质量分数为25%的H2SO4 ④新开封的Na2SO3粉末 ⑤硫化亚铁(块状固体,不溶于水)⑥NaOH溶液 ⑦溴水 ⑧Na2CO3溶液
在实验开始后不久即在B瓶中出现固体粉状物质。试完成下列问题:
(1)A中分液漏斗盛放的试剂是__________,烧瓶中盛放的试剂是__________。其实验开始时反应的化学方程式是_______________________________________。
(2)B中反应的化学方程式是______________________,反应的氧化产物与还原产物的物质的量之比是______________。
(3)E(启普发生器)中盛放的两种试剂发生反应的化学方程式是____________________。
(4)如果A、E两装置气体生成的速度相同,流量也相同,在D中发生反应的化学方程式是_______________________________________。
(5)D的作用是________________________,C的作用是________________________。
| ||
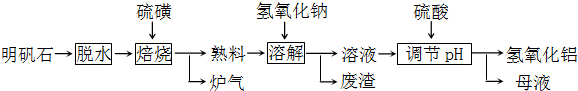
(12分) 明矾石的主要成分是K2SO4·Al2(SO4)3·2Al 2O3·6H2O,此外还含有少量Fe2O3杂质。利用明矾石制备氢氧化铝的流程如下: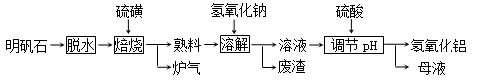
回答下列问题:
(1)“焙烧”过程中发生的反应为2Al2(SO4)3+3S  2Al 2O3+9SO2,其中氧化剂为 。
2Al 2O3+9SO2,其中氧化剂为 。
(2)“溶解”时反应的离子方程式为 。
(3)“调节pH”后过滤、洗涤Al(OH)3沉淀,证明已洗涤干净的实验操作和现象是
。
(4)调节pH时使用的是质量浓度(单位体积溶液所含溶质的质量)为882 g/L 的H2SO4 ,配制1L该溶液,需用量筒量取质量分数为98﹪的硫酸(密度是1.8g/cm3)
mL
(5)“废渣”、“母液”中可回收的物质分别是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com