
题目列表(包括答案和解析)
按要求回答下列问题:某有机物的一个分子含50个电子.
(1)若它为烃,则它的分子式可能为________;如果该烃在一定条件下不能与氢气反应,且该烃的一氯代物只有两种同分异构体,则该烃的结构简式为________.
(2)若它为含碳、氢、氧的有机物,它的分子式可能有________.(同一个碳原子上连接两个-OH的结构不稳定)
请按要求回答下列问题:
今有三种化合物结构如下:

(1)请写出丙中含氧官能团的名称: 。
(2)请判断上述哪些化合物互为同分异构体: 。
(3)写出化合物乙与小苏打溶液反应的化学方程式: 。
(4)请按酸性由强至弱排列甲、乙、丙的顺序: 。



| 棉球 | 棉球上滴加的试剂 | 实验现象 | 解释或结论 |
| i | 品红溶液 品红溶液 |
棉球变为白色,微热后又恢复红色 | |
| ii | FeCl3溶液 FeCl3溶液 |
棉球变为浅绿色 | 离子方程式: SO2+2Fe3++2H2O=2Fe3++SO42ˉ+4H+ SO2+2Fe3++2H2O=2Fe3++SO42ˉ+4H+ 结论: SO2有还原性 SO2有还原性 |
| iii | Na2S溶液 | 棉球变为浅黄色 | 解释:浅黄色物质是 S S 结论: SO2有氧化性 SO2有氧化性 |
| iv | 石蕊试液 石蕊试液 |
棉球变为红色 | 化学方程式: SO2+H2O?H2SO3 SO2+H2O?H2SO3 结论:该气体属于酸性氧化物 |
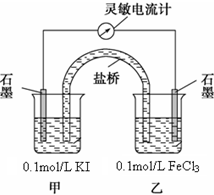 某研究性学习小组为证明2Fe3++2I-?2Fe2++I2为可逆反应(即反应存在一定的限度),设计如下几种方案.已知FeF63-是一种无色的稳定的络离子.
某研究性学习小组为证明2Fe3++2I-?2Fe2++I2为可逆反应(即反应存在一定的限度),设计如下几种方案.已知FeF63-是一种无色的稳定的络离子.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com