
题目列表(包括答案和解析)

甲:因为氯气与NaOH溶液反应,使溶液碱性减弱甚至呈酸性,所以溶液红色褪去。乙:因为氯气溶于水并与水反应生成HClO,由于HClO的氧化漂白作用而使溶液褪色。?
(1)验证甲同学的推测是否正确的方法是:________________________________。?
验证乙同学的推测是否正确的方法是:________________________。?
(2)如果将NaOH溶液改成KMnO4酸性溶液,把Cl2换成SO2气体,试问用图示所给装置完成喷泉实验是否合理?________(填“合理”或“不合理”)。?
如果认为不合理,请说明你的理由________________________________________________________。?
(3)类似“褪色喷泉实验”还有多种“变色的喷泉实验”,请你按实验要求,分别设计1个“变色喷泉实验”并填写下列表格:
编号 | 实验要求 | 烧杯中的溶液 | 滴管中的液体 | 烧瓶中的气体 |
① | 无色变红色喷泉 |
| H2O |
|
② | 红色变无色喷泉 |
|
| SO2 |

甲:因为氯气与NaOH溶液反应,使溶液碱性减弱甚至呈酸性,所以溶液红色褪去。乙:因为氯气溶于水并与水反应生成HClO,由于HClO的氧化漂白作用而使溶液褪色。
(1)验证甲同学的推测是否正确的方法是:____________________。
验证乙同学的推测是否正确的方法是:______________________。
(2)如果将NaOH溶液改成KMnO4酸性溶液,把Cl2换成SO2气体,试问用图示所给装置完成喷泉实验是否合理? _____________(填“合理”或“不合理”)。如果认为不合理,请说明你的理由______________________________。
(3)类似“褪色喷泉实验”还有多种“变色的喷泉实验”,请你按实验要求,分别设计1个“变色喷泉实验”并填写下列表格:
编号 | 实验要求 | 烧杯中的溶液 | 滴管中的液体 | 烧瓶中的气体 |
① | 无色变红色喷泉 |
| H2O |
|
② | 红色变无色喷泉 |
|
| SO2 |

图1-5-30
甲:因为氯气与NaOH溶液反应,使溶液碱性减弱甚至呈酸性,所以溶液红色褪去。
乙:因为氯气溶于水并与水反应生成HClO,由于HClO的氧化漂白作用而使溶液褪色。
(1)验证甲同学的推测是否正确的方法是;验证乙同学的推测是否正确的方法是_____________________________________________________________________。
(2)如果将NaOH溶液改成酸性KMnO4溶液,把Cl2换成SO2气体,试问用图示所给装置完成喷泉实验是否合理?__________ (填“合理”或“不合理”)。如果认为不合理,请说明你的理由:_____________________________________________________________________。
(3)类似“褪色喷泉实验”还有多种“变色的喷泉实验”。请你按实验要求,分别设计1个“变色喷泉实验”,并填写下列表格:
编号 | 实验要求 | 烧杯中的溶液 | 滴管中的液体 | 烧瓶中的气体 |
① | 无色变红色的喷泉 |
| H2O |
|
② | 红色变无色的喷泉 |
|
| SO2 |
(4)有人设计用钠做喷泉实验的装置(如图1-5-31所示,大头钉上是足够量的金属钠),其原理是_______________。实验过程中发现开始时喷出的喷泉压力大,水流急,但随后越来越慢,并且烧瓶不能充满溶液,若钠是足够量的,装置也不漏气,请说明原因:________________
____________________________________________________________________。

图1-5-31
某研究性学习小组设计了如下二组实验:
(I)实验验证元素周期律中, 非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。设计了如下图装置以验证氮、碳、硅元素的非金属性强弱。
设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:
A: ,B: ,C: 。
(2)写出烧杯中发生反应的离子方程式: 。
(Ⅱ )为比较Fe3+和Cu2+对H2O2的催化效果,甲、乙两位同学分别设计了如图一、图二所示的实验。
(1)图一可通过观察
定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是 ,或者将FeCl3溶液改成物质的量浓度为 mol/L的Fe2(SO4)3溶液。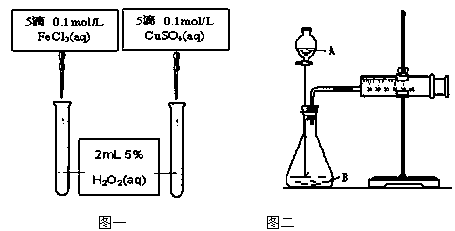
(2)检查图二装置气密性的方法是 ;
图二所示实验中需测量的数据是 。
某研究性学习小组的同学为验证浓硫酸与铜能反应而稀硫酸不能,设计了如图所示装置进行探究:将6.4 g 铜片和含0.2 moL溶质的18.4 mol/L浓硫酸放在圆底烧瓶中共热,直到无气体生成为止。(假定在此过程溶液体积不变)

(1)甲同学认为要证实上述结论,还应进行稀硫酸与铜片混合加热实验,你认为有无必要,并说明理由:________________
(2)下列试剂中能够用来进一步证明反应结束后的烧瓶中确有余酸的是:_____
A.铁粉 ?????? B.钠 ???? ?? C.氯化钡溶液 ???????? D.银粉
(3)为定量测定余酸的物质的量浓度,甲、乙两位同学进行了如下设计:
Ⅰ甲同学设想:在A装置增加一个导管通氮气驱赶气体(假定生成的气体全部逸出),先测定生成的SO2的量,然后计算剩余硫酸的浓度。他设计了如下二种方案来测定SO2的量:
方案① 将产生的气体缓缓通入足量用稀硫酸酸化的KMnO4溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀。
方案② 将气体缓缓通入足量硝酸钡溶液中,然后过滤、洗涤、干燥、称量沉淀。
经仔细分析后,发现有不合理之处,请填写下表(可以不填满):
序号 | 不合理的原因 | 误差 (偏低或偏高) | 改变措施 |
方案① |
|
|
|
方案② |
|
|
|
Ⅱ乙学生设计的方案是:分离出反应后的溶液并加蒸馏水稀释至1000 mL,取20.00 mL于锥形瓶中,滴入2~3滴酚酞指示剂,用标准NaOH溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),这种方法能否求出余酸的浓度,理由是_______________________________________。
(4)请再设计其他可行的实验方案,来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算,不必写操作细节)_____________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com