
题目列表(包括答案和解析)
 如图是元素周期表中1~20号元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:
如图是元素周期表中1~20号元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:

| ||
| △ |
| ||
| △ |
| ||
| ||
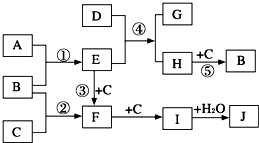 (2009?开封一模)如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).
(2009?开封一模)如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).
| ||
| ||
| x的取值范围 | 用x表示的y值表示式 |
| 烷烃名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 |
| 沸点(℃) | -88.6 | -42.1 | -0.5 | 36.1 |
| *燃烧热(kJ?mol-1) | 1560.7 | 2219.2 | 2877.6 | 3535.6 |
| A、正庚烷在常温常压下肯定不是气体 |
| B、烷烃的燃烧热和其所含碳原子数成线性关系 |
| C、随着烷烃中碳原子数增加,烷烃的沸点逐渐升高 |
| D、随着烷烃中氢元素的质量分数增大,烷烃的燃烧热逐渐增大 |
含有2~5个碳原子的直链烷烃沸点和燃烧热的数据见表:
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com