£®2013?≥ؗ٫¯∂˛ƒ££©ƒ≥ µ—È–°◊È∞—CO
2Õ®»Î±•∫ÕNa
2CO
3»Ð“∫÷∆»°NaHCO
3£¨◊∞÷√»ÁÕºÀ˘ 森∆¯√Ж‘“—ºÏ—È£¨≤ø∑÷º–≥÷◊∞÷√¬‘£©£∫
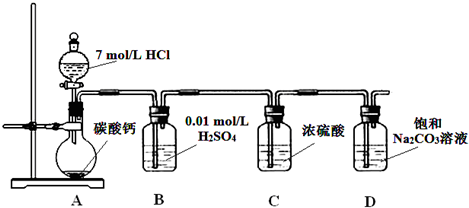
£®1£©D÷–≤˙…˙NaHCO
3µƒªØ—ß∑Ω≥Ã Ω «
Na2CO3+CO2+H2O®T2NaHCO3
Na2CO3+CO2+H2O®T2NaHCO3
£Æ
£®2£©«ÎΩ·∫œªØ—ß∆Ω∫‚“∆∂Ø‘≠¿ÌΩ‚ ÕB÷–»Ð“∫µƒ◊˜”√
CO2‘⁄ÀÆ÷–¥Ê‘⁄∆Ω∫‚£∫CO2+H2O?H2CO3?HCO3-+H+£¨”–H2SO4¥Ê‘⁄ ±£¨ø… π…œ ˆ∆Ω∫‚œÚ◊Û“∆∂Ø£¨¥”∂¯ºı…ŸCO2‘⁄ÀÆ÷–µƒ»ÐΩ‚£¨Õ¨ ±Œ¸ ’ª”∑¢≥ˆ¿¥µƒHCl∆¯ÃÂ
CO2‘⁄ÀÆ÷–¥Ê‘⁄∆Ω∫‚£∫CO2+H2O?H2CO3?HCO3-+H+£¨”–H2SO4¥Ê‘⁄ ±£¨ø… π…œ ˆ∆Ω∫‚œÚ◊Û“∆∂Ø£¨¥”∂¯ºı…ŸCO2‘⁄ÀÆ÷–µƒ»ÐΩ‚£¨Õ¨ ±Œ¸ ’ª”∑¢≥ˆ¿¥µƒHCl∆¯ÃÂ
£Æ
£®3£©µ±D÷–”–¥Û¡ø∞◊…´πÃÃÂŒˆ≥ˆ ±£¨Õ£÷π µ—È£¨Ω´πÃÃÂπ˝¬À°¢œ¥µ”°¢∏…‘Ô±∏”√£ÆŒ™»∑∂®πÃõƒ≥…∑÷£¨ µ—È–°◊ȅ˺∆∑Ω∞∏»Áœ¬£®≥∆»°“ª∂®÷ ¡øµƒπÃã¨≈‰≥…1000mL»Ð“∫◊˜Œ™—˘“∫£¨∆‰”ýπÃñ∏”√£©£∫
¢Ÿ∑Ω∞∏1£∫»°—˘“∫”Î≥Œ«ÂµƒCa£®OH£©
2»Ð“∫ªÏ∫œ£¨≥ˆœ÷∞◊…´≥¡µÌ£Æ µ—È–°◊È∂‘œ÷œÛ≤˙…˙µƒ‘≠¿ÌΩ¯––∑÷Œˆ£¨»œŒ™∏√∑Ω∞∏≤ª∫œ¿Ì£¨¿Ì”… «
Na2CO3∫ÕNaHCO3∂ºƒÐ∏˙Ca£®OH£©2»Ð“∫∑¢…˙∑¥”¶…˙≥…∞◊…´≥¡µÌ£¨ŒÞ∑®»∑∂®πÃõƒ≥…∑÷÷– «∑Ò∫¨”–NaHCO3
Na2CO3∫ÕNaHCO3∂ºƒÐ∏˙Ca£®OH£©2»Ð“∫∑¢…˙∑¥”¶…˙≥…∞◊…´≥¡µÌ£¨ŒÞ∑®»∑∂®πÃõƒ≥…∑÷÷– «∑Ò∫¨”–NaHCO3
£Æ
¢⁄∑Ω∞∏2£∫»°—˘“∫”ÎBaCl
2»Ð“∫ªÏ∫œ£¨≥ˆœ÷∞◊…´≥¡µÌ≤¢”–∆¯ÃÂ≤˙…˙£Æ µ—È–°◊È»œŒ™πÃÃÂ÷–¥Ê‘⁄NaHCO
3£¨∆‰¿Î◊”∑Ω≥Ã Ω «
2HCO3-+Ba2+=BaCO3°˝+CO2°¸+H2O
2HCO3-+Ba2+=BaCO3°˝+CO2°¸+H2O
£Æ∏√–°◊È»œŒ™≤ªƒÐ»∑∂® «∑ҥʑ⁄Na
2CO
3£¨ƒ„»œŒ™∏√Ω·¬€ «∑Ò∫œ¿Ì£ø
∫œ¿Ì
∫œ¿Ì
£Æ
¢€∑Ω∞∏3£∫ µ—È–°◊È÷–º◊°¢““Õ¨—ß¿˚”√NaHCO
3µƒ≤ªŒ»∂®–‘Ω¯––»Áœ¬ µ—È£∫
º◊Õ¨—ߣ∫»°—˘“∫400mL£¨”√pHº∆≤‚»Ð“∫pH£¨‘ŸÀÆ‘°º”»»’Ù∑¢÷¡200mL£¨Ω”œ¬¿¥µƒ≤Ÿ◊˜ «
¿‰»¥µΩ “Œ¬£¨º”ÀÆ÷¡»Ð“∫ê˝Œ™400mL£¨‘Ÿ¥Œ≤‚∂®pH
¿‰»¥µΩ “Œ¬£¨º”ÀÆ÷¡»Ð“∫ê˝Œ™400mL£¨‘Ÿ¥Œ≤‚∂®pH
£¨Ω·π˚±Ì√˜∞◊…´πÃÃÂ÷–¥Ê‘⁄NaHCO
3£ÆŒ™Ω¯“ª≤Ω÷§√˜∞◊…´πÃà«∑ÒŒ™¥ø檵ƒNaHCO
3£¨Ω·∫œº◊Õ¨—ß µ—È£¨ªπ”¶≤π≥‰µƒ µ—È «
»°œýÕ¨÷ ¡øµƒ¥ø檵ƒNaHCO3≈‰≥…1000mL»Ð“∫£¨»°400mL£¨÷ÿ∏¥º◊µƒ µ—È£¨Ω¯––∂‘’’
»°œýÕ¨÷ ¡øµƒ¥ø檵ƒNaHCO3≈‰≥…1000mL»Ð“∫£¨»°400mL£¨÷ÿ∏¥º◊µƒ µ—È£¨Ω¯––∂‘’’
£Æ
““Õ¨—ߣ∫¿˚”√“«∆˜≤‚∂®¡ÀπÃÃÂ≤–¡Ù¬
(≤–¡Ù¬ =| £”ýπÃõƒ÷ ¡ø | ‘≠ ºπÃõƒ÷ ¡ø |
°¡100%)ÀÊŒ¬∂»±‰ªØµƒ«˙œþ£¨»ÁÕºÀ˘ æ£Æ
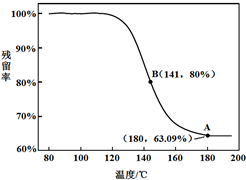
a£Æ∏˘æðAµ„◊¯±Íµ√µΩµƒΩ·¬€ «
∞◊…´πÃÃÂŒ™NaHCO3
∞◊…´πÃÃÂŒ™NaHCO3
£Æ
b£Æ∏˘æðBµ„◊¯±Í£¨º∆À„≤–¡ÙπÃÃÂ÷–n£®NaHCO
3£©£∫n£®Na
2CO
3£©=
1.7
1.7
£Æ
Õ®π˝…œ ˆ µ—È£¨∏√–°◊È»œŒ™£¨ø…“‘œÚ±•∫ÕNa
2CO
3»Ð“∫÷–Õ®»Îπ˝¡øCO
2÷∆±∏NaHCO
3£Æ


