2SO
2(g)+O
2(g)?2SO
3(g),反应过程的能量变化如图所示.已知1mol SO
2(g)氧化为1mol SO
3(g)的△H=-99kJ/mol.
请回答下列问题:
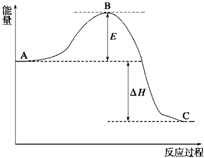
(1)图中A、C分别表示
反应物能量
反应物能量
、
生成物能量
生成物能量
,E的大小对该反应的反应热有无影响?
没有影响
没有影响
.该反应通常用V
2O
5作催化剂,加V
2O
5会使图中B点升高还是降低
降低
降低
,理由是
因为催化剂改变了反应历程,使活化能E降低
因为催化剂改变了反应历程,使活化能E降低
;
(2)图中△H=
-198
-198
kJ/mol;
(3)V
2O
5的催化循环机理可能为:V
2O
5氧化SO
2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化.写出该催化循环机理的化学方程式
SO2+V2O5═SO3+2VO2,4VO2+O2═2V2O5
SO2+V2O5═SO3+2VO2,4VO2+O2═2V2O5
;
(4)已知单质硫的燃烧热为296kJ/mol,写出硫燃烧的热化学方程式:
S(s)+O2(g)=SO2(g)△H=-296 kJ/mol
S(s)+O2(g)=SO2(g)△H=-296 kJ/mol
,计算由3mol S(s)生成3mol SO
3(g)的△H=
-1185 kJ/mol
-1185 kJ/mol
.

 (2009?辽宁)2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.
(2009?辽宁)2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.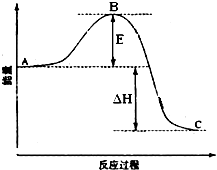 2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.请回答下列问题:
2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.请回答下列问题: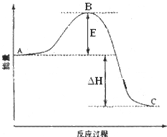 2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:
2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题: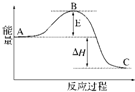 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.请回答下列问题:
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.请回答下列问题: 2SO2(g)+O2(g)?2SO3(g),反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.
2SO2(g)+O2(g)?2SO3(g),反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.