
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЃЈ1ЃЉаДГіЩЯЪіФкШнЩцМАЕФЛЏбЇЗНГЬЪНЁЃ
ЃЈ2ЃЉжЦШЁМзЙшЭщЕФзАжУгыжЦШЁ________ЃЈЬюЁАбѕЦјЁБЁАЧтЦјЁБЛђЁАТШЦјЁБЃЉЕФзАжУЯрЫЦЁЃ
ЃЈ3ЃЉМгШыЯЁбЮЫсжЎЧАгІЯђУмБезАжУжаЭЈШывЛЛсЖљЕЊЦјЃЌЦфФПЕФЪЧ______________ЁЃ
ЃЈ4ЃЉЪеМЏМзЙшЭщЦјЬхжЛФмВЩгУ________ЗЈЃЌетЪЧвђЮЊ________ЁЃЪеМЏЭъМзЙшЭщЦјЬхКѓВЛФмжБНгНЋЕМЦјЙмДгЫЎВлжаШЁГіЃЌетЪЧЮЊСЫЗРжЙ________ЃЌе§ШЗЕФВйзїЗНЗЈЪЧ________________ЁЃ
ЃЈ5ЃЉЮЊСЫбаОПМзЙшЭщЕФЛЏбЇаджЪЃЌНјааШчЯТЪЕбщЃКЂйНЋМзЙшЭщЭЈШыЩйСПЕФИпУЬЫсМиЫсадШмвКжаЃЌЗЂЯжгаЖўбѕЛЏУЬЩњГЩЃЌЭЌЪБЛЙЩњГЩСЫЫљгаЦјЬхжазюЧсЕФЦјЬхЃЌШЛКѓОВтЖЈЕУжЊЫљЕУШмвКЮЊЮоЩЋЕФЙшЫсМиЃЈK2SiO3ЃЉШмвКЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊ_______________________ЁЃЂкНЋМзЙшЭщЭЈШыЩйСПЕФЯѕЫсвјШмвКЃЌЗЂЯжгаГСЕэЩњГЩЃЌШЛКѓОВтЖЈЕУжЊГСЕэЮЊЛьКЯЮяЃЌЦфжагаЖўбѕЛЏЙшЁЃЯђГфЗжЗДгІКѓЕФШмвКжаЕЮШыМИЕЮЯЁбЮЫсЃЌЮДЗЂЯжгаАзЩЋГСЕэЩњГЩЃЛЯђЗДгІКѓЕФдШмвКжаЕЮШыМИЕЮЬМЫсФЦШмвКЃЌШДЗЂЯжгаЦјХнбИЫйЗХГіЁЃдђНЋМзЙшЭщЭЈШыЯѕЫсвјШмвКжаЃЌЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ____________________________________ЁЃ
ЃЈ6ЃЉжЦЭъМзЙшЭщКѓЃЌМьбщзАжУжаЪЧЗёгаВаСєЕФМзЙшЭщЕФЗНЗЈЪЧ_________________________ЁЃ
ЃЈ1ЃЉжЦШЁбѕЦј
ЂйгУ20ЃЅЕФH2O2ШмвКЃЌЭЈЙ§ЗДгІ2H2O2![]() 2H2O+O2ЁќРДжЦШЁбѕЦјЃЌдђдкЯТСаAЁЂBЁЂCШ§зАжУжазюМбзАжУЪЧ_____________ЃЛ
2H2O+O2ЁќРДжЦШЁбѕЦјЃЌдђдкЯТСаAЁЂBЁЂCШ§зАжУжазюМбзАжУЪЧ_____________ЃЛ
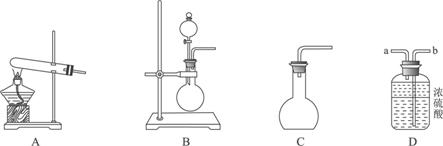
ЂкгыЦјЬхЗЂЩњзАжУЯрСЌНгЕФDзАжУЕФЕМЙмПкЪЧ_____________ЃЛ
ЂлЮЊСЫФмЪЙВњЩњЕФбѕЦјБЛГфЗжИЩдяЃЌПЩВЩШЁЕФВйзїЪЧ______________________________ЁЃ
ЃЈ2ЃЉжЦШЁбѕЛЏЭ
НЋm gЭЗлдкбѕЦјСїжаМгШШЕНИпЮТЃЌЪЙЭЗлШЋВПбѕЛЏЃЌЕУn gЗлФЉXЁЃввЭЌбЇВщдФзЪСЯжЊЃКЭгыбѕЦјЕФЗДгІгаЃКЂй2Cu+O2![]() 2CuOЃЌЂк4CuO
2CuOЃЌЂк4CuO![]() 2Cu2O+O2ЁќЃЛдкЫсадЬѕМўЯТЃК2Cu+(aq)====Cu(s)+Cu2+(aq)ЁЃгЩДЫЕУГіНсТлЃКЭЫфШЛШЋВПбѕЛЏЃЌЕЋгЩгкМгШШЮТЖШЦЋИпЃЌВњЮяВЂВЛвЛЖЈЪЧДПCuOЃЌПЩФмКЌгавЛЖЈСПЕФбѕЛЏбЧЭЃЈCu2OЃЉЁЃ
2Cu2O+O2ЁќЃЛдкЫсадЬѕМўЯТЃК2Cu+(aq)====Cu(s)+Cu2+(aq)ЁЃгЩДЫЕУГіНсТлЃКЭЫфШЛШЋВПбѕЛЏЃЌЕЋгЩгкМгШШЮТЖШЦЋИпЃЌВњЮяВЂВЛвЛЖЈЪЧДПCuOЃЌПЩФмКЌгавЛЖЈСПЕФбѕЛЏбЧЭЃЈCu2OЃЉЁЃ
ЃЈ3ЃЉЬНОПЭЕФбѕЛЏЮяЕФГЩЗж
ЮЊВтЖЈЗлФЉXжаЪЧЗёКЌгаCu2OЃЌМзЁЂввЁЂБћШ§ЭЌбЇЗжБ№ЩшМЦШчЯТЪЕбщЗНАИЁЃ
МзЭЌбЇЕФЪЕбщЗНАИЪЧЃКЯђЗлФЉXжаМгШыЯЁСђЫсЃЌШєга_____________ЃЌдђЫЕУїЙЬЬхжаКЌгаCu2OЁЃ
ввЭЌбЇЕФЪЕбщЗНАИЪЧЃКдйНЋЗлФЉXЗХШыбѕЦјжаМгШШЃЌШчЙћЦфжЪСПдіМгЃЌдђЫЕУїЦфжаКЌгаCu2OЁЃ
БћЭЌбЇЕФЪЕбщЗНАИЪЧЃКЭЈЙ§ЗжЮіЪЕбщЪ§ОнОЭПЩвдШЗЖЈЗлФЉXЕФГЩЗжЁЃ
ШєnЕФШЁжЕЗЖЮЇЪЧ__________ЁмnЃМ__________ЃЌдђЗлФЉXжаКЌгаCu2OЃЌЦфЮяжЪЕФСПЪЧ__________ЁЃ
ЧыФудйЩшМЦвЛИігыЩЯЪіШ§ИіЪЕбщЗНАИжаЯжЯѓВЛЭЌЕФЪЕбщЗНАИЃЌЭЈЙ§ЖдЛЏбЇЗДгІКЭЖдЪЕбщЯжЯѓЕФЗжЮіРДШЗЖЈЗлФЉXжаЪЧЗёКЌгаCu2OЁЃаДГіИУЪЕбщжаРызгЗДгІЕФЗНГЬЪНЁЃ
МзЭЌбЇЩшМЦвдЯТЪЕбщжЦШЁбѕЦјКЭбѕЛЏЭЁЃ
ЃЈ1ЃЉжЦШЁбѕЦј
ЂйгУ20ЃЅЕФH2O2ШмвКЃЌЭЈЙ§ЗДгІ2H2O2MnO22H2OЃЋO2ЁќРДжЦШЁбѕЦјЃЌдђдкЯТСаAЁЂBЁЂCШ§зАжУжазюМбзАжУЪЧ______
 |
ЂкгыЦјЬхЗЂЩњзАжУЯрСЌНгЕФDзАжУЕФЕМЙмПкЪЧ______
ЂлЮЊСЫФмЪЙВњЩњЕФбѕЦјБЛГфЗжИЩдяЃЌПЩВЩШЁЕФВйзїЪЧ
_________________________________________________________________________________
ЃЈ2ЃЉжЦШЁбѕЛЏЭ
НЋm gЭЗлдкбѕЦјСїжаМгШШЕНИпЮТЃЌЪЙЭЗлШЋВПбѕЛЏЃЌЕУn gЗлФЉXЁЃввЭЌбЇВщдФзЪСЯжЊЃКЭгыбѕЦјЕФЗДгІгаЃКЂй2CuЃЋO2Ёї\s\up2 (ЁЊЁЊ2CuOЃЌЂк4CuOЃО1000Ёц2Cu2OЃЋO2ЁќЃЛдкЫсадЬѕМўЯТЃК2CuЃЋ(aq)ЁЊЁЊCu(s)ЃЋ
Cu2ЃЋ(aq)ЁЃгЩДЫЕУГіНсТлЃКЭЫфШЛШЋВПбѕЛЏЃЌЕЋгЩгкМгШШЮТЖШЦЋИпЃЌВњЮяВЂВЛвЛЖЈЪЧДПCuOЃЌПЩФмКЌгавЛЖЈСПЕФбѕЛЏбЧЭЃЈCu2OЃЉЁЃ
ЃЈ3ЃЉЬНОПЭЕФбѕЛЏЮяЕФГЩЗж
ЮЊВтЖЈЗлФЉXжаЪЧЗёКЌгаCu2OЃЌМзЁЂввЁЂБћШ§ЭЌбЇЗжБ№ЩшМЦШчЯТЪЕбщЗНАИЁЃ
МзЭЌбЇЕФЪЕбщЗНАИЪЧЃКЯђЗлФЉXМгШыЯЁСђЫсЃЌШєга ЃЌдђЫЕУїЙЬЬхжаКЌгаCu2OЁЃ
ввЭЌбЇЕФЪЕбщЗНАИЪЧЃКдйНЋЗлФЉXЗХШыбѕЦјжаМгШШЃЌШчЙћЦфжЪСПдіМгЃЌдђЫЕУїЦфжаКЌгаCu2OЁЃ
БћЭЌбЇЕФЪЕбщЗНАИЪЧЃКЭЈЙ§ЗжЮіЪЕбщЪ§ОнОЭПЩвдШЗЖЈЗлФЉXЕФГЩЗжЁЃ
ШєnЕФШЁжЕЗЖЮЇЪЧ ЁмnЃМ_____ЃЌдђЗлФЉXжаКЌгаCu2OЃЌЦфЮяжЪЕФСПЪЧ___________ЁЃ
ЧыФудйЩшМЦвЛИігыЩЯЪіШ§ИіЪЕбщЗНАИжаЯжЯѓВЛЭЌЕФЪЕбщЗНАИЃЌЭЈЙ§ЖдЛЏбЇЗДгІКЭЖдЪЕбщЯжЯѓЕФЗжЮіРДШЗЖЈЗлФЉXжаЪЧЗёКЌгаCu2OЁЃаДГіИУЪЕбщжаРызгЗДгІЕФЗНГЬЪНЁЃ
МзЭЌбЇЩшМЦвдЯТЪЕбщжЦШЁбѕЦјКЭбѕЛЏЭЁЃ
(1)жЦШЁбѕЦј
ЂйгУ20ЃЅЕФ![]() ШмвКЃЌЭЈЙ§ЗДгІ
ШмвКЃЌЭЈЙ§ЗДгІ![]() РДжЦШЁбѕЦјЃЌдђдкЯТСаAЁЂBЁЂCШ§зАжУжазюМбзАжУЪЧ_____
РДжЦШЁбѕЦјЃЌдђдкЯТСаAЁЂBЁЂCШ§зАжУжазюМбзАжУЪЧ_____

ЂкгыЦјЬхЗЂЩњзАжУЯрСЌНгЕФDзАжУЕФЕМЙмПкЪЧ_____
ЂлЮЊСЫФмЪЙВњЩњЕФбѕЦјБЛГфЗжИЩдяЃЌПЩВЩШЁЕФВйзїЪЧ
(2)жЦШЁбѕЛЏЭ
НЋm gЭЗлдкбѕЦјСїжаМгШШЕНИпЮТЃЌЪЙЭЗлШЋВПбѕЛЏЃЌЕУn gЗлФЉXЁЃввЭЌбЇВщдФзЪСЯжЊ: ЭгыбѕЦјЕФЗДгІгаЃКЂй![]() ЃЌЂк
ЃЌЂк![]() ЃЛдкЫсадЬѕМўЯТЃК
ЃЛдкЫсадЬѕМўЯТЃК![]() ЁЃгЩДЫЕУГіНсТлЃКЭЫфШЛШЋВПбѕЛЏЃЌЕЋгЩгкМгШШЮТЖШЦЋИпЃЌВњЮяВЛвЛЖЈЪЧДПCuOЃЌПЩФмКЌгавЛЖЈСПЕФбѕЛЏбЧЭ(
ЁЃгЩДЫЕУГіНсТлЃКЭЫфШЛШЋВПбѕЛЏЃЌЕЋгЩгкМгШШЮТЖШЦЋИпЃЌВњЮяВЛвЛЖЈЪЧДПCuOЃЌПЩФмКЌгавЛЖЈСПЕФбѕЛЏбЧЭ(![]() )ЁЃ
)ЁЃ
(3)ЬНОПЭЕФбѕЛЏЮяЕФГЩЗж
ЮЊВтЖЈЗлФЉXжаЪЧЗёКЌга![]() ЃЌМзЁЂввЁЂБћШ§ЭЌбЇЗжБ№ЩшМЦШчЯТЪЕбщЗНАИЁЃ
ЃЌМзЁЂввЁЂБћШ§ЭЌбЇЗжБ№ЩшМЦШчЯТЪЕбщЗНАИЁЃ
МзЭЌбЇЕФЪЕбщЗНАИЪЧЃКЯђЗлФЉXжаМгШыЯЁСђЫсЃЌШєга___ ЃЌдђЫЕУїЙЬЬхжаКЌга![]() ЁЃ
ЁЃ
ввЭЌбЇЕФЪЕбщЗНАИЪЧЃКдйНЋЗлФЉXЗХШЫбѕЦјжаМгШШЃЌШчЙћЦфжЪСПдіМгЃЌдђЫЕУїЦфжаКЌга![]() ЁЃ
ЁЃ
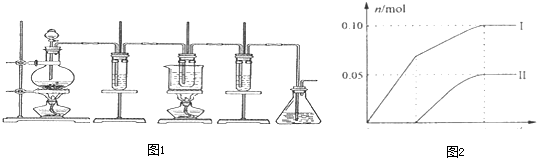
БћЭЌбЇЕФЪЕбщЗНАИЪЧЃКЭЈЙ§ЗжЮіЪЕбщЪ§ОнОЭПЩвдШЗЖЈЗлФЉXЕФГЩЗжЁЃШєnЕФШЁжЕЗЖЮЇЪЧ![]() ЃЌдђЗлФЉXжаКЌга
ЃЌдђЗлФЉXжаКЌга![]() ЃЌЦфЮяжЪЕФСПЪЧ_____ЁЃ
ЃЌЦфЮяжЪЕФСПЪЧ_____ЁЃ
ЧыФудйЩшМЦвЛИігыЩЯЪіШ§ИіЪЕбщЗНАИжаЯжЯѓОљВЛЯрЭЌЕФЪЕбщЗНАИЃЌЭЈЙ§ЖдЛЏбЇЗДгІКЭЖдЪЕбщЯжЯѓЕФЗжЮіРДШЗЖЈЗлФЉXжаЪЧЗёКЌга![]() ЁЃаДГіИУЪЕбщжаЗДгІЕФРызгЗНГЬЪНЁЃ
ЁЃаДГіИУЪЕбщжаЗДгІЕФРызгЗНГЬЪНЁЃ
| ||
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com