
题目列表(包括答案和解析)
F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂,都极易与水发生反应,其中6XeF4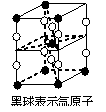
+12H2O === 2XeO3+4Xe↑+24HF+3O3↑,下列推测正确的是
A.XeF2分子中各原子均达到8原子的稳定结构
B.某种氟化氙的晶体结构单元如右图所示,可推测其化学式为XeF6
C.XeF4按上述方式水解,每生成4molXe转移16mol电子
D.XeF2加入水中,在水分子的作用下,将重新生成Xe和F2
|
F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次递增),都极易与水反应.其中6XeF4+12H2O | |
| [ ] | |
A. |
XeF2分子中各原子均达到八电子的稳定结构 |
B. |
某种氟化氙的晶体结构单元如图所示,可推知其化学式为XeF6
|
C. |
XeF4按已知方式水解,每生成2 mol Xe转移8 mol电子 |
D. |
XeF2加入水中,在水分子的作用下,将重新生成Xe和F2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com