ЪЕбщЪвгавЛЦПNa
2SO
3ЙЬЬхЃЌПЩФмКЌгаNaClЁЂNa
2SO
4ЁЂBaCl
2ЁЂK
2CO
3ЁЂK
2SO
4жаЕФвЛжжЛђМИжждгжЪЃЌЭЈЙ§ЯТСаЪЕбщШЗЖЈИУбљЦЗЕФГЩЗжМАNa
2SO
3ЕФжЪСПЗжЪ§ЃЎ
ЂйШЁЩйСПбљЦЗгкЪдЙмжаЃЌМгЫЎеёЕДЃЌЮДМћГСЕэЩњГЩЃЛ
ЂкЭИЙ§РЖЩЋюмВЃСЇЙлВьЃЌбцЩЋЗДгІЮозЯЩЋЃЛ
ЂлгУгвЭМЫљЪОвЧЦїНјааКЯРэзщзАЃЌВтЖЈВњЩњЦјЬхЕФЬхЛ§ЃЈSO
2дкСђЫсжаЕФШмНтКіТдВЛМЦЃЉ
ЧыЛиД№ЯТСаЮЪЬтЃК
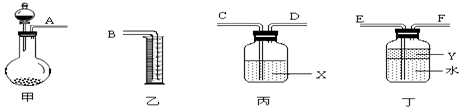
ЃЈ1ЃЉАДЦјСїДгзѓЕНгвЗНЯђЃЌе§ШЗЕФСЌНгЫГађЮЊЃКAНг
ЃЌ
Нг
ЃЌ
НгBЃЎ
ЃЈ2ЃЉРћгУЫљзщзАжУЃЌгЩЗжвКТЉЖЗЯђдВЕзЩеЦПжаЕЮМг10mLЫЎЃЌНЋХХШыСПЭВжа
mLвКЬхЃЎ
ЃЈ3ЃЉвКЬхXЪЧ
ЃЌЦфзїгУЪЧ
ЃЎ
ЃЈ4ЃЉYЕФзїгУЪЧЗРжЙВњЩњЕФЦјЬхШмгкЫЎЃЌЯТСаЫљИјЪдМСЗћКЯвЊЧѓЕФЪЧ
ЃЎ
AЃЎБНBЃЎЫФТШЛЏЬМCЃЎОЦОЋDЃЎЦћгЭ
ШєГЦШЁбљЦЗ3.00gЃЌМгШы10.0mol/LЕФСђЫсжСЙ§СПЃЈЙВ5mLЃЉЃЌВњЩњЮоЩЋЦјЬхЃЌХХШыСПЭВжавКЬхЕФЬхЛ§ЮЊ229mLЃЈБъзМзДПіЃЉЃЎ
ЃЈ5ЃЉЖдЛёЕУзМШЗЕФЦјЬхЬхЛ§ЮовцЕФВйзїга
ЃЈЬюађКХЃЉ
ЂйМьВщзАжУЕФЦјУмадЃЛ
ЂкСЌЭЈввЁЂЖЁЕФЕМЙмвЊдЄЯШзЂТњЫЎЃЛ
ЂлЖСЪ§ЪБЪгЯпгыСПЭВФкАМвКУцзюЕЭЕуЯрЦНЃЛ
ЂмЛжИДЕНЪвЮТКѓдйЩЯЯТЕїећСПЭВЮЛжУЃЌЪЙввЁЂЖЁСНвКУцЯрЦНЃЛ
ЂндкМззАжУНКШћЩЯдйСЌНгвЛИіЕМЙмЃЌЭЈШыN
2НЋЯЕЭГжаSO
2ШЋВПХХГіЃЎ
ЃЈ6ЃЉЯђвнГіЦјЬхКѓЕФШмвКжаМгШыЩдЙ§СПЕФBaCl
2ШмвКЃЌЙ§ТЫЁЂЯДЕгЁЂИЩдяЃЌЕУЕНАзЩЋГСЕэ13.98gЃЎИљОнЪЕбщЫљЕУЯжЯѓМАЪ§ОнЃЌПЩжЊЃКбљЦЗжаNa
2SO
3ЕФжЪСПЗжЪ§ЪЧ
ЃЌКЌгаЕФдгжЪЪЧ
ЃЎ

