AΓΔBΓΔCΓΔD «÷–―ßΜ·―ßΒΡ≥ΘΦϊΈο÷ Θ§Τδ÷–AΓΔBΓΔCΨυΚ§”–Ά§“Μ÷÷‘ΣΥΊΘ°‘Ύ“ΜΕ®ΧθΦΰœ¬œύΜΞΉΣΜ·ΒΡΙΊœΒ»γΆΦΥυ ΨΘ®≤ΩΖ÷Ζ¥”Π÷–ΒΡH
2O“―¬‘»ΞΘ©Θ°
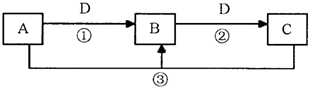
«κΧνΩ’ΘΚ
Θ®1Θ©»τD «…ζ≤ζΓΔ…ζΜν÷–”ΟΝΩΉν¥σΓΔ”ΟΆΨΉνΙψΒΡΫπ τΒΞ÷ Θ§Φ”»»’τΗ…BΒΡ»ή“Κ≤ΜΡήΒΟΒΫBΘ§‘ρBΒΡΜ·―ß ΫΩ…Ρή «
FeCl3
FeCl3
Θ®÷Μ–¥“Μ÷÷Θ©Θ°”Ο”–ΙΊάκΉ”ΖΫ≥Χ ΫΫβ Ά B»ή“Κœ‘Υα–‘ΒΡ‘≠“ρ «ΘΚ
¬»Μ·ΧζΥ°ΫβΕχ ΙΤδ»ή“Κ≥ Υα–‘
¬»Μ·ΧζΥ°ΫβΕχ ΙΤδ»ή“Κ≥ Υα–‘
Θ°
Θ®2Θ©»τA «“Μ÷÷Φν–‘ΤχΧεΘ§≥Θ”ΟΉς÷ΤάδΦΝΘ§BΚΆDΈΣΩ’ΤχΒΡ÷ς“Σ≥…Ζ÷Θ§‘ρΖ¥”ΠΔΎΒΡΜ·―ßΖΫ≥Χ ΫΈΣ
Θ°
Θ®3Θ©»τDΒΡ¬»ΦνΙΛ“ΒΒΡ÷ς“Σ≤ζΤΖΘ§B”–ΝΫ–‘Θ§‘ρΖ¥”ΠΔΎΒΡάκΉ”ΖΫ≥Χ Ϋ «
AlΘ®OHΘ©3+OH-®TAlO2-+2H2O
AlΘ®OHΘ©3+OH-®TAlO2-+2H2O
Θ°
Θ®4Θ©»τDΈΣΥαΜρΥα–‘ΤχΧεΘ§‘ρAΓΔCΩ…“‘ «
NaOHΓΔNaHCO3ΜρFeΓΔFeΘ®NO3Θ©3
NaOHΓΔNaHCO3ΜρFeΓΔFeΘ®NO3Θ©3
Θ®«κΑ¥Υ≥–ρ–¥≥ω»Έ“β“ΜΉιΖϊΚœ“Σ«σΒΡΈο÷ ΒΡΜ·―ß ΫΘ©
Θ®5Θ©»τC «“Μ÷÷Έ¬ “ΤχΧεΘ§D «Ω’ΤχΒΡ÷ς“Σ≥…Ζ÷÷°“ΜΘ§1molΚΎ…ΪΙΧΧεAΆξ»Ϊ»Φ…’Ζ≈≥ω393.5kJ»»ΝΩΘ§1molBΤχΧεΆξ»Ϊ»Φ…’Ζ≈≥ω283.0kJ»»ΝΩΘ§‘ρAΓζBΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣ
2CΘ®sΘ©+O2Θ®gΘ©®T2COΘ®gΘ©ΓςH=-221kJ?mol-1
2CΘ®sΘ©+O2Θ®gΘ©®T2COΘ®gΘ©ΓςH=-221kJ?mol-1
Θ°



