实验是进行科学探究的重要方式,请根据下图回答问题:

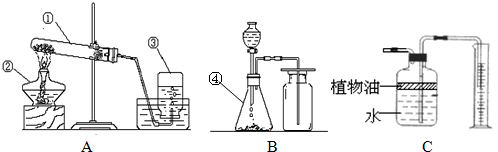
(1)用A图所示装置进行电解水实验时,a管产生的气体是
氢气
氢气
,检验a管产生气体的方法是
燃着的木条去点燃,气体能燃烧,产生淡蓝色火焰
燃着的木条去点燃,气体能燃烧,产生淡蓝色火焰
,b管接电源的
正
正
极.某学习小组的同学测定了两管逸出气体的体积,记录如下:
| 实 验 时 间/min |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
… |
| a管中气体体积/mL |
6 |
12 |
20 |
29 |
39 |
49 |
59 |
69 |
… |
| b管中气体体积/mL |
2 |
4 |
7 |
1l |
16 |
21 |
26 |
31 |
… |
请回答:理论上a管和b管中气体的体积比为
2:1
2:1
;虽然装置气密性良好、读数正确,但电解开始阶段两管气体的体积比
大于
大于
(填“大于”或“小于”)理论比值,不符合理论比值的原因是
氧气微溶于水,氢气难溶于水;部分氧气可能与电极反应了
氧气微溶于水,氢气难溶于水;部分氧气可能与电极反应了
.
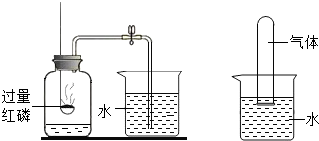
(2)用B图所示的装置测定空气中氧气的含量,实验的现象有
红磷在瓶内燃烧,产生浓厚的白烟;打开止水夹后,水倒流入集气瓶且约占集气瓶剩余容积的
红磷在瓶内燃烧,产生浓厚的白烟;打开止水夹后,水倒流入集气瓶且约占集气瓶剩余容积的
若实测结果偏低,其原因可能是
装置漏气或红磷量不足或未冷却到室温就打开了止水夹
装置漏气或红磷量不足或未冷却到室温就打开了止水夹
(只写一条).
(3)C图实验中集气瓶底部装水的目的是
防止生成物溅落炸裂集气瓶
防止生成物溅落炸裂集气瓶
.

 空气主要是由氮气和氧气组成的混合物,请你参与研究性小组有关空气成分测定和性质的实验探究.
空气主要是由氮气和氧气组成的混合物,请你参与研究性小组有关空气成分测定和性质的实验探究.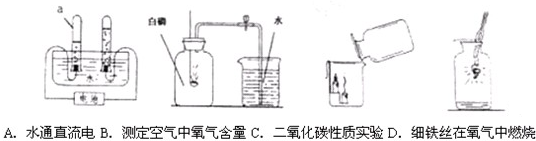


 氯化钙(固)+氨气+水.
氯化钙(固)+氨气+水.