
题目列表(包括答案和解析)
| 1 |
| 2 |
| 1 | 2 |
乙醇可通过淀粉等生物质原料发酵制得,属于可再生资源,通过乙醇制取氢气具有良好的应用前景。已知通过乙醇制取氢气有如下两条路线:
a.水蒸气催化重整:CH3CH2OH(g) +H2O(g)®4H2(g) +2CO(g) DH =+255.58 kJ·mol-1
b.部分催化氧化:CH3CH2OH(g)+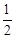 O2(g)®3H2(g)+2CO(g)
DH =+13.76kJ·mol-1
O2(g)®3H2(g)+2CO(g)
DH =+13.76kJ·mol-1
则下列说法错误的是( )
A.从原料消耗的角度来看,a路线制氢更有价值
B.从能量消耗的角度来看,b路线制氢更加有利
C.a路线制氢由于要消耗很多能量,所以在实际生产中意义不大
D.按b路线进行,体系的能量会降低
乙醇可通过淀粉等生物质原料发酵制得,属于可再生资源,由乙醇制取氢气具有良好的应用前景。已知由乙醇制取氢气可有如下两条路线:
① 水蒸气催化重整:
CH3CH2OH(g)+H2O(g)====4H2(g)+2CO(g) ![]() 255.58 kJ?mol
255.58 kJ?mol![]()
② 部分催化氧化:
CH3CH2OH(g)+1/2 O2(g)====3H2(g)+2CO(g)![]() 13.76 kJ?mol
13.76 kJ?mol![]()
请回答下列问题:
(1)下列说法正确的是 。(填字母)
A.从原料消耗的角度来看,路线①制氢更有价值
B.从能量消耗的角度来看,路线①制氢更加有利
C.由于路线②制氢要消耗很多能量,故在实际生产中意义不大
D.路线①和路线②均使用催化剂,是为了降低反应所需的能量
(2)在体积为1 L的密闭容器中充入2 mol CO和4 mol H2,一定条件下发生反应:
4H2(g)+2CO(g)![]() CH3CH2OH(g)+H2O(g)
CH3CH2OH(g)+H2O(g) ![]() 255.58kJ?mol
255.58kJ?mol![]()
欲使![]() (CH3CH2OH)/
(CH3CH2OH)/![]() (CO)增大,应采取措施是 。(答两项即可)
(CO)增大,应采取措施是 。(答两项即可)
(3)若用0.8lt淀粉为原料,理论上可制得质量分数为92%的乙醇溶液 t。
(4)若用乙醇得到的合成气(CO、H2的混合气)来合成一种生物汽油。乙醇按路线① 和路线② 的反应各占50%,合成气合成生物汽油的反应为:![]()
假定这种生物汽油中含有X、Y两种成分,且X、Y都是含8个碳原子的烃,X是苯的同系物,Y是烷烃。1 t质量分数为92%的乙醇经上述转化(假定各步转化率均为100%),最终可得到X的质量为多少吨?
 O2(g)®3H2(g)+2CO(g) DH =+13.76kJ·mol-1
O2(g)®3H2(g)+2CO(g) DH =+13.76kJ·mol-1| A.从原料消耗的角度来看,a路线制氢更有价值 |
| B.从能量消耗的角度来看,b路线制氢更加有利 |
| C.a路线制氢由于要消耗很多能量,所以在实际生产中意义不大 |
| D.按b路线进行,体系的能量会降低 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com