ИљОнШчЭМЫљЪОЪЕбщЃЌЛиД№ЯТСаЮЪЬтЃЎ
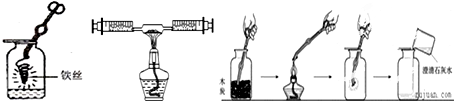
AЁЂЬњЫПдкбѕЦјжаШМЩе BЁЂВтЖЈПеЦјжабѕЦјЕФЬхЛ§ЗжЪ§ЁЁ CЁЂФОЬПдкбѕЦјжаШМЩе
ЃЈ1ЃЉЭМAжаЗДгІЕФЮФзжБэДяЪНЮЊ
ЃЛЬњЫПвЊШЦГЩТна§зДЕФдвђЪЧ
Бугкв§ШМЬњЫП
Бугкв§ШМЬњЫП
ЃЛМЏЦјЦПжадЄЯШМгЫЎЛђЯИЩГЕФзїгУЪЧ
ЗРжЙЩњГЩЕФШлЛЏЮяНІТфеЈСбЦПЕз
ЗРжЙЩњГЩЕФШлЛЏЮяНІТфеЈСбЦПЕз
ЃЎШєНЋбѕЦјЛЛГЩПеЦјЃЌдђИУЛЏбЇЗДгІ
ВЛФм
ВЛФм
ЃЈЬюЁАФмЁБЛђЁАВЛФмЁБЃЉНјааЃЌЦфдвђЪЧ
ПеЦјжабѕЦјХЈЖШЬЋЕЭ
ПеЦјжабѕЦјХЈЖШЬЋЕЭ
ЃЎ
ЃЈ2ЃЉЭМBжаКьСзЗДгІЕФЮФзжБэДяЪНЮЊ
ЃЛдкЪЕбщЕФМгШШЙ§ГЬжаЃЌНЛЬцЛКТ§ЭЦЖЏСНИізЂЩфЦїЕФФПЕФЪЧ
ЪЙПеЦјжаЕФбѕЦјгыКьСзГфЗжЗДгІ
ЪЙПеЦјжаЕФбѕЦјгыКьСзГфЗжЗДгІ
ЃЛЩЯЪіЪЕбщжЛЪЧДжТдВтЖЈПеЦјжабѕЦјКЌСПЕФвЛжжЗНЗЈЃЌФуШЯЮЊдьГЩИУЪЕбщВЛЙЛОЋШЗЕФПЩФмдвђЪЧ
КьСзЕФСПВЛзу
КьСзЕФСПВЛзу
ЁЂ
зАжУЦјУмадВЛКУ
зАжУЦјУмадВЛКУ
ЃЈаДСНЬѕМДПЩЃЉЃЎ
ЃЈ3ЃЉгУлсліЧЏМаШЁвЛаЁПщФОЬПЗХдкОЦОЋЕЦЛ№бцЕФ
Этбц
Этбц
ВПЗжбИЫйЩеКьЃЛЭМжаЪЂЗХбѕЦјЕФЦППкИЧЩЯВЃСЇЦЌЕФФПЕФЪЧ
ЗРжЙбѕЦјРЉЩЂ
ЗРжЙбѕЦјРЉЩЂ
ЃЎ
ЃЈ4ЃЉзіФОЬПдкбѕЦјжаШМЩеЕФЪЕбщЪБЃЌФОЬПШМЩеЕФЯжЯѓЪЧ
ЗЂГіАзЙтЁЂЗХГіШШСПЁЂЩњГЩФмЪЙГЮЧхЪЏЛвЫЎБфЛызЧЕФЦјЬх
ЗЂГіАзЙтЁЂЗХГіШШСПЁЂЩњГЩФмЪЙГЮЧхЪЏЛвЫЎБфЛызЧЕФЦјЬх
ЃЎ

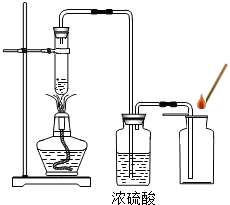 ФГбЇаЃЛЏбЇаЫШЄаЁзщЭЌбЇдкбЇЯАСЫжЦШЁбѕЦјетвЛНкФкШнКѓЃЌЗЂЯждкЪЕбщЪвРягУ5%H2O2ШмвКМгШШжЦO2ЃЌгУДјЛ№аЧЕФФОЬѕМьбщЃЌФОЬѕКмФбИДШМЃЎЭЌбЇУЧОЙ§ШЯецЙлВьЃЌВТЯыЦфПЩФмдвђЪЧ
ФГбЇаЃЛЏбЇаЫШЄаЁзщЭЌбЇдкбЇЯАСЫжЦШЁбѕЦјетвЛНкФкШнКѓЃЌЗЂЯждкЪЕбщЪвРягУ5%H2O2ШмвКМгШШжЦO2ЃЌгУДјЛ№аЧЕФФОЬѕМьбщЃЌФОЬѕКмФбИДШМЃЎЭЌбЇУЧОЙ§ШЯецЙлВьЃЌВТЯыЦфПЩФмдвђЪЧ
