
题目列表(包括答案和解析)
A.0.1 B.0.4 C.0.2 D.0.3
可逆反应:X(g)+3 Y(g) 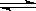 2 R(g)+2W(g)在4种不同情况下的反应速率分别如下,其中表示该反应速率最快的是( )
2 R(g)+2W(g)在4种不同情况下的反应速率分别如下,其中表示该反应速率最快的是( )
A.v(X) = 0.15 mol·(L·S)-1 B.v(Y) = 0.60 mol·(L·S)-1
C.v(R) = 8.0 mol·(L·min)-1 D.v(W) = 0.45 mol·(L·S)-1
化学反应A(g)+3B(g) 2C(g)+2D(g),在下列四个选项中是不同的情况下测得的不同物质的反应速率,其中表示该化学反应的反应速率最快的是
2C(g)+2D(g),在下列四个选项中是不同的情况下测得的不同物质的反应速率,其中表示该化学反应的反应速率最快的是
A.υ(D)=0.6 mol/(L·min) B.υ(B)=0.45 mol/ (L·s)
C.υ(C)=0.40 mol/ (L·min) D.υ(A)=0.2mol/ (L·s)
1909年丹麦科学家Sorensen用公式pH=-lgc(H+)引入pH,1999年荷兰科学家HenK
Van Lubeck提出酸度(AG)的概念,以更好地表示溶液的酸碱性。酸度(AG)的定义为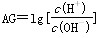 。 下列有关叙述中错误的是( )
。 下列有关叙述中错误的是( )
A.常温时,中性溶液的pH=7,AG=0
B.酸性溶液的AG>0,AG越大,溶液的pH越小
C.碱性溶液的AG>0,AG越大,溶液的pH越大
D.常温下,0.1 mol/LNaOH溶液,AG=-12,pH=13
反应:3A(g)+B(g)===2C(g)+2D(g),在不同条件下,用不同物质表示其反应速率,分别为:
①v(A)=0.6 mol/(L·min); ②v(B)=0.45 mol/(L·min);
③v(C)=0.015 mol/(L·min); ④v(D)=0.45 mol/(L·min)。
则此反应在不同条件下进行最快的是
A.②③ B.①③ C.②④ D.②
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com