
题目列表(包括答案和解析)
 、AlO2-、K+、S2-等离子
、AlO2-、K+、S2-等离子下列溶液中有关判断正确的是( )
A.常温下pH = 2的HA溶液与pH = 12的MOH溶液任意比混合:
C (H+) + c (M+) = c (OH-) + c (A-)
B.pH相等的CH3COONa、 NaOH和Na2CO3三种溶液:
C (NaOH) < c (CH3COONa) < c (Na2CO3)
C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:
C (CH3COO-) + 2c (OH-) = 2c (H+) + c (CH3COOH)
D. 0.1 mol / L的NaHA溶液,其pH = 4:c (HA-) > c (H+) > c (H2A) > c (A2-)
(11分)工业上制备BaCl2的工艺流程图如图7:
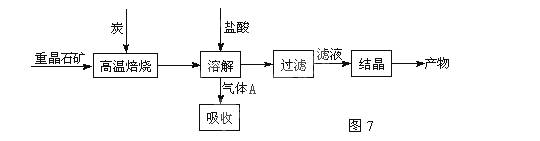
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。
已知:BaSO4(s) + 4C(s)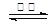 4CO(g) + BaS(s) △H1 =
+571.2 kJ·mol-1 ①
4CO(g) + BaS(s) △H1 =
+571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s)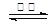 2CO2(g) + BaS(s) △H2= +226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2= +226.2 kJ·mol-1 ②
(1)高温焙烧时常把原料粉碎,目的是_________________________________
(2)常温下,相同浓度的Na2S和NaHS溶液中,说法正确的是: (3分)
A. Na2S溶液的pH比NaHS溶液pH大
B. 两溶液中含有的离子种类不同
C. 两溶液中滴入同体积同浓度的盐酸,产生气体速率相等
D. 两溶液中加入NaOH固体,c(S2-)都增大
E. NaHS溶液中:c(Na+) > c(HS-)> c(OH-) > c(H+) > c(S2-)
(3)反应C(s) + CO2(g)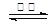 2CO(g)的△H =
2CO(g)的△H =
(4)制备BaCl2的工艺流程图中气体A用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为:
(5)实际生产中必须加入过量的炭,同时还要通入空气,目的是:
(写出一种原因即可)
(11分)工业上制备BaCl2的工艺流程图如图7:
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。
已知:BaSO4(s) + 4C(s)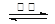 4CO(g) + BaS(s) △H1 =" +571.2" kJ·mol-1 ①
4CO(g) + BaS(s) △H1 =" +571.2" kJ·mol-1 ①
BaSO4(s) + 2C(s)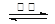 2CO2(g) + BaS(s) △H2=" +226.2" kJ·mol-1 ②
2CO2(g) + BaS(s) △H2=" +226.2" kJ·mol-1 ②
(1)高温焙烧时常把原料粉碎,目的是_________________________________
(2)常温下,相同浓度的Na2S和NaHS溶液中,说法正确的是: (3分)
| A.Na2S溶液的pH比NaHS溶液pH大 |
| B.两溶液中含有的离子种类不同 |
| C.两溶液中滴入同体积同浓度的盐酸,产生气体速率相等 |
| D.两溶液中加入NaOH固体,c(S2-)都增大 |
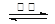 2CO(g)的△H =
2CO(g)的△H = 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com