铁是日常生活中最常见的金屑之一.某班同学在学习铁的知识时,有下列问题:
问题1:铁为何称为黑色金属?
问题2:Fe
20
3在髙温下能否分解为FeO和O
2?
问题3:在加热条件下,铁对甲醇的氧化能否起催化作用?
(1)对于问题1,同学们在网上査寻到两种解释:
A.因为在铁表面上有黑色的铁的氧化物,所以叫黑色金屑.
B.因为铁的粉末为黑色,铁的氧化物也为黑色,所以叫黑色金属.
你认为正确的说法是______(填代号).若有一黑色粉末,为铁和四氧化三铁的混合物,请设计一个实验方案证明其中有Fe
3O
4______
(2)对于问题2,同学们准备进行实验探究,设计了两种方案:
A.将Fe
2O
3放在坩埚中高温灼烧,观察灼烧前后颜色是否变化.
B.将Fe
2O
3放在坩埚中髙温灼烧,称量灼烧前后质量是否变化.
回答下列问题:
①方案A中,如果高温灼烧后______ (填颜色变化),说明Fe
2O
3确实发生了变化.能否说明生成的物质一定为FeO?______(填“能“或“否”);
②方案B中,测得固体灼烧前后质量之比为30:29(假设固体灼烧后完全分解),则髙温灼烧后生成固体物质是______.比较两种方案,你认为较好的方案是______;
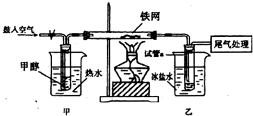
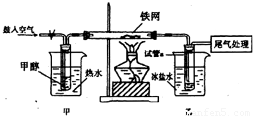
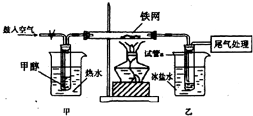
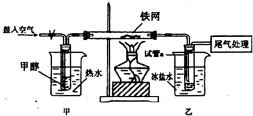
(3)对于问题3,同学们设计了如下实验进行探究.回答相关问题:
①实验过程中铁网出现银白色和黑色交替的现象,写出甲醇反应的化学方程式(假设铁网上出现的黑色物为FeO)______;
②甲水浴加热的作用是______;
③反应一段时间后,试管a中收集到的物质可能有______.

 铁是日常生活中最常见的金屑之一.某班同学在学习铁的知识时,有下列问题:
铁是日常生活中最常见的金屑之一.某班同学在学习铁的知识时,有下列问题: