
题目列表(包括答案和解析)
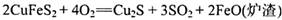 ;③制粗铜,在1200°C发生的主要反应为:
;③制粗铜,在1200°C发生的主要反应为: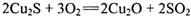 ;
;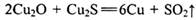 ;④电解精炼。
;④电解精炼。| A.②③两步所涉及的反应全部是氧化还原反应 |
B.由6mol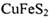 生成6molCu,反应共消耗15mol 02 生成6molCu,反应共消耗15mol 02 |
C.反应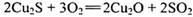 中: 中: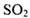 只是氧化产物 只是氧化产物 |
| D.电解精炼时,粗铜应与外电源正极相连 |
铜的冶炼大致可分为:①富集:将硫化物矿进行浮选;
②焙烧,主要反应为:2CuFeS2+4O2=Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1200℃发生的主要反应为:
2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6Cu+SO2↑;
④电解精炼。
下列说法正确的是 ( )
A.上述灼烧过程的尾气均可直接排入空气
B.由6mol CuFeS2生成6mol Cu,反应共消耗15mol O2
C.反应2Cu2O+Cu2S=6Cu+SO2↑中,氧化剂只有Cu2O
D.电解精炼时,粗铜应与外电源正极相连
铜的冶炼大致可分为:①富集:将硫化物矿进行浮选;
②焙烧,主要反应为:2CuFeS2+4O2=Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1200℃发生的主要反应为:
2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6Cu+SO2↑;
④电解精炼。
下列说法正确的是 ( )
A.上述灼烧过程的尾气均可直接排入空气
B.由6mol CuFeS2生成6mol Cu,反应共消耗15mol O2
C.反应2Cu2O+Cu2S=6Cu+SO2↑中,氧化剂只有Cu2O
D.电解精炼时,粗铜应与外电源正极相连
铜的冶炼大致可分为:①富集:将硫化物矿进行浮选;②培烧,主要反应为: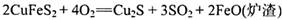 ;③制粗铜,在1200°C发生的主要反应为:
;③制粗铜,在1200°C发生的主要反应为: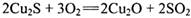 ;
;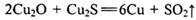 ;④电解精炼。
;④电解精炼。
下列说法错误的是( )
| A.②③两步所涉及的反应全部是氧化还原反应 |
B.由6mol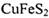 生成6molCu,反应共消耗15mol 02 生成6molCu,反应共消耗15mol 02 |
C.反应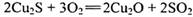 中: 中: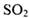 只是氧化产物 只是氧化产物 |
| D.电解精炼时,粗铜应与外电源正极相连 |
| A、上述灼烧过程的尾气均可直接排空 | B、上述过程中,由6molCuFeS2制取6molCu时共消耗12molO2 | C、在反应2Cu2O+Cu2S=6Cu+SO2↑中,只有Cu2O作氧化剂 | D、电解精炼铜时,粗铜应与外接电源的正极相连接 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com