
题目列表(包括答案和解析)
(15分)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)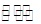 CH3OH(g)。
CH3OH(g)。
(1)下图是该反应在不同温度下CO的转化率随时间变化的曲线。
①该反应的焓变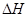 0(填“>”、“<”或“=”)。
0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1 K2(填“>”、“<”或“=”)。
③若容器容积不变,下列措施可增加甲醇产率的是 。
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
(2)已知在常温常压下
①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)
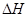 =-akJ·mol-1
=-akJ·mol-1
②2CO(g)+O2(g)=2CO2(g)
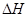 =-bkJ·mol-1
=-bkJ·mol-1
③H2O(g)=H2O(1)
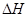 =-ckJ·mol-1
=-ckJ·mol-1
则,CH3(OH)(1)+O2(g)=CO(g)+2H2O(1)
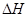 = kJ·mol-1
= kJ·mol-1
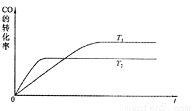
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。
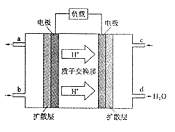
①该电池工作时,b口通入的物质为 ,c口通入的
物质为 。
②该电池正极的电极反应式为: 。
③工作一段时间后,当6.4g甲醇完全反应生成CO2时,
有 NA个电子转移。
(4)以上述电池做电源,用下图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示):
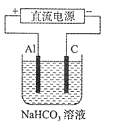
, 。
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
(1)下图是该反应在不同温度下CO的转化率随时间变化的曲线。
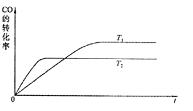
①该反应的焓变![]() 0(填“>”、“<”或“=”)。
0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1 K2(填“>”、“<”或“=”)。
③若容器容积不变,下列措施可增加甲醇产率的是 。
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
(2)已知在常温常压下
①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g) ![]() =-akJ·mol-1
=-akJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ![]() =-bkJ·mol-1
=-bkJ·mol-1
③H2O(g)=H2O(1) ![]() =-ckJ·mol-1
=-ckJ·mol-1
则,CH3(OH)(1)+O2(g)=CO(g)+2H2O(1) ![]() = kJ·mol-1
= kJ·mol-1
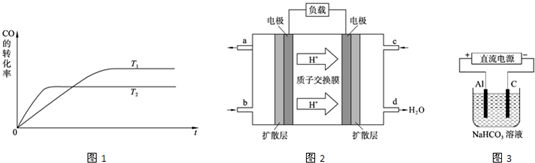
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。
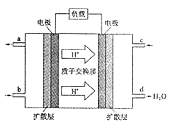
①该电池工作时,b口通入的物质为 ,c口通入的
物质为 。
②该电池正极的电极反应式为: 。
③工作一段时间后,当6.4g甲醇完全反应生成CO2时,
有 NA个电子转移。
(4)以上述电池做电源,用下图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示):
, 。
(15分)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)CH3OH(g)。
(1)下图是该反应在不同温度下CO的转化率随时间变化的曲线。
①该反应的焓变 0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1 K2(填“>”、“<”或“=”)。
③若容器容积不变,下列措施可增加甲醇产率的是 。
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
(2)已知在常温常压下
①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g) =-akJ·mol-1
②2CO(g)+O2(g)=2CO2(g) =-bkJ·mol-1
③H2O(g)=H2O(1) =-ckJ·mol-1
则,CH3(OH)(1)+O2(g)=CO(g)+2H2O(1) = kJ·mol-1
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。
①该电池工作时,b口通入的物质为 ,c口通入的
物质为 。
②该电池正极的电极反应式为: 。
③工作一段时间后,当6.4g甲醇完全反应生成CO2时,
有 NA个电子转移。
(4)以上述电池做电源,用下图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示):
, 。
| [CH3OH] |
| [CO][H2]2 |
| [CH3OH] |
| [CO][H2]2 |
| b-a-4c |
| 2 |
| b-a-4c |
| 2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com