
(2011?新余二模)化学--选修物质结构与性质
已知:A、B、C、D、E、F五种元素核电荷数依次增大,属周期表中前四周期的元素.其中A原子核外有三个未成对电子;化合物B
2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满.请根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为
Na<Al<Si<N
Na<Al<Si<N
.(用元素符号表示)
(2)B的氯化物的熔点比D的氯化物的熔点
高
高
(填高或低),理由是
NaCl为离子晶体而SiCl4为分子晶体
NaCl为离子晶体而SiCl4为分子晶体
.
(3)E的最高价氧化物分子的空间构型是
平面正三角形
平面正三角形
.
(4)F的核外电子排布式是
1s22s22p63s23p63d104s1(或[Ar]3d104s1)
1s22s22p63s23p63d104s1(或[Ar]3d104s1)
,F的高价离子与A的简单氢化物形成的配离子的化学式为
[Cu(NH3)4]2+
[Cu(NH3)4]2+
.
(5)A、F形成某种化合物的晶胞结构如图所示,则其化学式为
Cu3 N
Cu3 N
;(黑色球表示F原子)
(6)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为
共价键
共价键
.

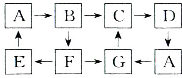
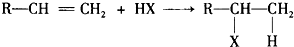
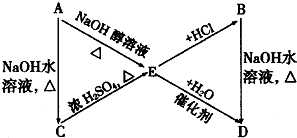




 +NaOH
+NaOH +NaCl
+NaCl +NaOH
+NaOH +NaCl
+NaCl


 (2011?新余二模)化学--选修物质结构与性质
(2011?新余二模)化学--选修物质结构与性质