
题目列表(包括答案和解析)



(1)_____________________________________、________________________________;
(2)______________________________________________________________。

(1)_____________________________________、________________________________;
(2)______________________________________________________________。
(10分)钨是高熔点金属,工业上用黑钨铁矿[(Fe,Mn)WO4]冶炼金属钨有多种方法,同时还可制得副产品高锰酸钾。已知WO3是钨的稳定氧化物,它不溶于水也不溶于酸,可用钨酸(H2WO4,黄色,不溶于水)或某些钨酸盐分解制得。其主要的工艺流程如下:
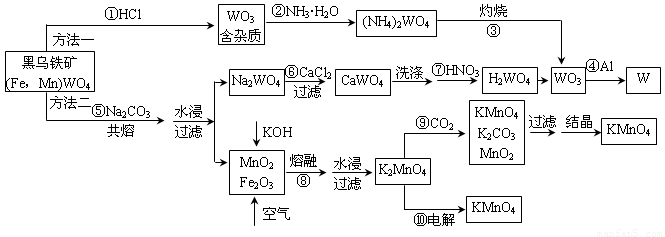
请根据图示及所学知识回答下列问题:
⑴写出反应④的化学方程式: ▲ 。
⑵写出反应⑨的离子方程式: ▲ 。
⑶方法二制WO3的过程中,需洗涤CaWO4,如何检验CaWO4已洗涤干净: ▲ 。
⑷整个工艺流程所涉及的物质中,属于酸性氧化物的有 ▲ 。
⑸写出反应⑩中阳极反应的电极反应式: ▲ 。
钨是高熔点金属,工业上用黑钨铁矿[(Fe,Mn)WO4]冶炼金属钨有多种方法,同时还可制得副产品高锰酸钾。已知WO3是钨的稳定氧化物,它不溶于水也不溶于酸,可用钨酸(H2WO4,黄色,不溶于水)或某些钨酸盐分解制得。其主要的工艺流程如下:
请根据图示及所学知识回答下列问题:
⑴写出反应④的化学方程式: ▲ 。
⑵写出反应⑨的离子方程式: ▲ 。
⑶方法二制WO3的过程中,需洗涤CaWO4,如何检验CaWO4已洗涤干净: ▲ 。
⑷整个工艺流程所涉及的物质中,属于酸性氧化物的有 ▲ 。
⑸写出反应⑩中阳极反应的电极反应式: ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com