ЬНОПвЛЃКЙЄвЕЬњКьЕФжївЊГЩЗжЪЧFe
2O
3ЃЌЛЙКЌгаЩйСПЕФFeOЁЂFe
3O
4ЃЎФГаЫШЄаЁзщгУВнЫсОЇЬхжЦШЁCOЃЌВЂНјааСЫШчЯТЭМЫљЪОЪЕбщЃЎ
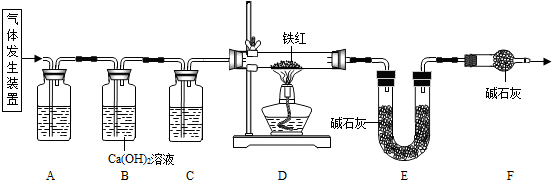
ЪдЛиД№ЃК
ЁОВщдФзЪСЯЁПВнЫсОЇЬхЃЈH
2C
2O
4?3H
2OЃЉдкХЈH
2SO
4зїгУЯТЪмШШЗжНтЩњГЩCO
2КЭCOЃЎ
ЃЈ1ЃЉЪЕбщЧАгІЯШ
МьВщзАжУЕФЦјУмад
МьВщзАжУЕФЦјУмад
ЃЎ
ЃЈ2ЃЉНјШыDжаЕФЦјЬхЪЧДПОЛЁЂИЩдяЕФCOЃЌдђAжаЪдМСЪЧ
c
c
ЁЂCжаЕФЪдМСЪЧ
a
a
ЃЈЬюзжФИБрКХЃЉЃЎ
aЃЎХЈСђЫс bЃЎГЮЧхЕФЪЏЛвЫЎ cЃЎЧтбѕЛЏФЦШмвК
ЃЈ3ЃЉFзАжУЕФзїгУЪЧ
ЗРжЙПеЦјжаЖўбѕЛЏЬМЁЂЫЎеєЦјНјШыEзАжУжа
ЗРжЙПеЦјжаЖўбѕЛЏЬМЁЂЫЎеєЦјНјШыEзАжУжа
ЃЎ
ЃЈ4ЃЉФГЭЌбЇШЯЮЊЭМЪОзАжУгаВЛзужЎДІЃЌИФНјЕФЗНЗЈЪЧ
дкFКѓгУОЦОЋЕЦЕуШМ
дкFКѓгУОЦОЋЕЦЕуШМ
ЃЎ
ЬНОПЖўЃКОЋЛЙдЬњЗлЪЧвЛжжживЊЕФЛЏЙЄдСЯЃЌФГаЫШЄаЁзщЖдЦфНјааЯТСабаОПЃК
ЁОЮяжЪжЦБИЁПРћгУТЬЗЏжЦБИОЋЛЙдЬњЗлЕФЙЄвеСїГЬШчЯТЃК

ДжЛЙдЬњЗлжаЛЙКЌгаЩйСПЬњЕФбѕЛЏЮяКЭFe
3CдгжЪЃЌПЩгУЧтЦјдкИпЮТЯТНјвЛВНЛЙдЃЌЦфЗДгІЗНГЬЪНЮЊFe
xO
y+y H
2x Fe+y H
2OЃЌFe
3C+2H
23Fe+CH
4ЃЎ
ЃЈ1ЃЉаДГіБКЩежабѕЛЏЬњгыCOЗДгІЕФЛЏбЇЗНГЬЪНЃК
ЃЎ
ЃЈ2ЃЉБКЩежаМгНЙЬПЕФзїгУГ§СЫПЩвдЩњГЩCOЭтЃЌЛЙФм
ЬсЙЉШШСП
ЬсЙЉШШСП
ЃЎ
ЁОКЌСПВтЖЈЁПЮЊЕУЕНОЋЛЙдЬњЗлВЂВтЖЈДжЛЙдЬњЗлжабѕКЭЬМдЊЫиЕФжЪСПЗжЪ§ЃЌАДШчЯТзАжУНјааЪЕбщЃЎ
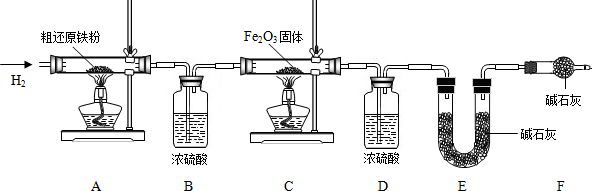
вбжЊ3CH
4+4Fe
2O
33CO
2+6H
2O+8FeЃЈМйЩшУПВНЗДгІЖМЭъШЋЃЌЧвВЛПМТЧзАжУФкдгаПеЦјЖдВтЖЈНсЙћЕФгАЯьЃЉЃЎ
ЃЈ3ЃЉжївЊЪЕбщВНжшШчЯТЃК
ЂйАДЫГађзщзАвЧЦїЃЌМьВщзАжУЕФЦјУмадЃЌГЦСПбљЦЗКЭБивЊзАжУЕФжЪСПЃЛ
ЂкЕуШМAДІОЦОЋЕЦЃЛ
ЂлЛКЛКЭЈШыДПОЛИЩдяЕФH
2ЃЛ
ЂмЕуШМCДІОЦОЋЕЦЃЛ
ЂнЗжБ№ЯЈУ№AДІЁЂCДІОЦОЋЕЦЃЛ
ЂодйЛКЛКЭЈШыЩйСПH
2ЃЛ
ЂпдйДЮГЦСПБивЊзАжУЕФжЪСПЃЎ
ВйзїЕФЯШКѓЫГађЪЧЂйЁњЂлЁњ
B
B
ЁњЂнЁњЂоЁњЂпЃЈЬюзжФИЃЉ
AЃЎЂкЁњЂмBЃЎЂмЁњЂк
ЃЈ4ЃЉВНжшЂлЕФФПЕФЪЧ
Г§ШЅзАжУФкЕФбѕЦјЃЌЗРжЙЗЂЩњБЌеЈ
Г§ШЅзАжУФкЕФбѕЦјЃЌЗРжЙЗЂЩњБЌеЈ
ЃЌбщжЄИУВНжшФПЕФДяЕНЕФЪЕбщЗНЗЈЪЧ
ЪеМЏЮВЦјППНќШМзХЕФОЦОЋЕЦЃЌЬ§Щљвє
ЪеМЏЮВЦјППНќШМзХЕФОЦОЋЕЦЃЌЬ§Щљвє
ЃЛ
ЃЈ5ЃЉШєШБЩйзАжУDЃЌдђЫљВтбѕдЊЫиЕФжЪСПЗжЪ§НЋ
ВЛБф
ВЛБф
ЃЈЬюЁАЦЋДѓЁЏЁЏЁАЦЋаЁЁАЛђЁАВЛБфЁАЃЌЯТЭЌЃЉЃЎ
ЃЈ6ЃЉДжЛЙдЬњЗлбљЦЗЕФжЪСПЮЊ20.000gЃЌзАжУBЁЂEЗжБ№діжи0.360gКЭ0.440gЃЌдђМЦЫубљЦЗГіжаЬМдЊЫиЕФжЪСПЗжЪ§ЪЧ
0.6%
0.6%
ЃЌбѕдЊЫиЕФжЪСПЗжЪ§ЪЧ
1.6%
1.6%
ЃЎЃЈЮоашМЦЫуЙ§ГЬЃЉЃЎ



