
题目列表(包括答案和解析)
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
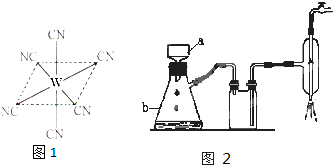
Ⅰ.2009年墨西哥、美国等地出现甲型H1N1流感疫情,引起全世界的关注,这种流感疫情是由甲型H1N1病毒引起的。美国疾病控制和预防中心推荐使用瑞士罗氏制药公司生产的“达菲”胶囊和英国葛兰素—史克公司生产的喷雾式药剂“乐感清”两款药物。
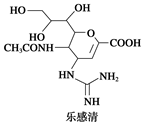
达菲和乐感清的结构简式如下图所示:

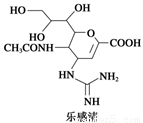
请回答下列问题:
(1)乐感清的分子式是____ 。
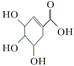
(2)合成达菲的主要原料莽草酸(结构简式为 
 )存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )
)存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )
A. 1 mol莽草酸与足量的金属钠反应可生成4mol H2。
B. 1 mol莽草酸与足量氢氧化钠溶液反应,最多可消耗氢氧化钠4 mol。
C. 1 mol莽草酸与足量的碳酸钠溶液反应可生成二氧化碳气体1 mol。
D. 1 mol莽草酸与足量的碳酸氢钠溶液反应可生成二氧化碳气体1 mol
(3)下列每组中各有三对物质,它们都能用分液漏斗分离的是
A.乙酸乙酯和水,酒精和水,植物油和水
B.四氯化碳和水,溴苯和水,硝基苯和水
C.甘油和水,乙酸和水,乙酸和乙醇
D.汽油和水,苯和水,乙二醇和水
Ⅱ.下图中A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3溶液发生反应,C和D的相对分子质量相等,且E为无支链的化合物。请回答下列问题:

(1)C分子中官能团的名称是 ;化合物B不能发生的反应是 (填字母序号)。
a.加成反应 b.取代反应 c.消去反应
d.酯化反应 e.水解反应 f.氧化反应
(2)反应②的化学方程式是___________________________。(3) A的结构简式是_________________。
(4)同时符合下列三个条件的B的同分异构体的数目有______个。
a含有间二取代苯环结构 b.属于非芳香酸酯 c.可与FeCl3溶液发生显色反应
写出其中任意一个同分异构体的结构简式__________________________________。
Ⅰ.2009年墨西哥、美国等地出现甲型H1N1流感疫情,引起全世界的关注,这种流感疫情是由甲型H1N1病毒引起的。美国疾病控制和预防中心推荐使用瑞士罗氏制药公司生产的“达菲”胶囊和英国葛兰素—史克公司生产的喷雾式药剂“乐感清”两款药物。
达菲和乐感清的结构简式如下图所示: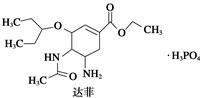

请回答下列问题:
(1)乐感清的分子式是____ 。
(2)合成达菲的主要原料莽草酸(结构简式为 
 )存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )
)存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )
A. 1 mol莽草酸与足量的金属钠反应可生成4mol H2。
B. 1 mol莽草酸与足量氢氧化钠溶液反应,最多可消耗氢氧化钠4 mol。
C. 1 mol莽草酸与足量的碳酸钠溶液反应可生成二氧化碳气体1 mol。
D. 1 mol莽草酸与足量的碳酸氢钠溶液反应可生成二氧化碳气体1 mol
(3)下列每组中各有三对物质,它们都能用分液漏斗分离的是
A.乙酸乙酯和水,酒精和水,植物油和水
B.四氯化碳和水,溴苯和水,硝基苯和水
C.甘油和水,乙酸和水,乙酸和乙醇
D.汽油和水,苯和水,乙二醇和水
Ⅱ.下图中A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3溶液发生反应,C和D的相对分子质量相等,且E为无支链的化合物。请回答下列问题:
(1)C分子中官能团的名称是 ;化合物B不能发生的反应是 (填字母序号)。
a.加成反应 b.取代反应 c.消去反应
d.酯化反应 e.水解反应 f.氧化反应
(2)反应②的化学方程式是___________________________。(3) A的结构简式是_________________。
(4)同时符合下列三个条件的B的同分异构体的数目有______个。
a含有间二取代苯环结构 b.属于非芳香酸酯 c.可与FeCl3溶液发生显色反应
写出其中任意一个同分异构体的结构简式__________________________________。
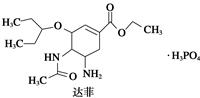
 )存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )
)存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )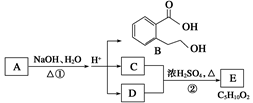
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com