
题目列表(包括答案和解析)
| a-b |
| 3 |
| b-a |
| 4 |
| b |
| 22.4 |
![]()
(1)气密性检查:请回答该装置气密性检查的最简单的方法:
_____________________________________________________________________。
(2)加入固体试剂Cu片,打开阀门K,拔出注射器活塞,加入一小片Cu片将注射器活塞装上并压至底部,排出里面的空气。
(3)吸取浓HNO3,将注射器尖嘴导管插入浓HNO3中,并向上拉注射器活塞吸取少量的浓HNO3,然后迅速关闭阀门K,请回答此时可能观察到的实验现象:______________________________________________________________,当生成的NO2气体体积接近最大刻度时,迅速打开阀门K,将反应液放入NaOH溶液中后关闭K。
Ⅱ.NO2性质实验
(1)观察收集到的气体呈____________色,若向下用力压活塞,发现气体的颜色先变深,后变浅,原因是__________________________________________________________________。
(2)为了验证进行实验(2)后注射器中的气体,请设计一实验方案加以验证:
______________________________________________________________。
Ⅲ.将盛有a mol NO2和b mol NO混合气体的试管倒立于水槽中,再通入c mol O2,充分反应后,试管里剩余气体的成分及物质的量决定于a、b和c的关系,请完成下面表格。
a、b和c的关系 | 剩余气体的成分 | 剩余气体的物质的量 |
4c=a+3b |
|
|
|
| (a+3b-4c)/3 |
| O2 |
|
亚硝酸钠(NaNO2)是重要的防腐剂。某化学兴趣小组尝试制备亚硝酸钠,查阅资料:①HNO2为弱酸,在酸性溶液中,NO2-可将MnO4-还原为Mn2+且无气体生成。
②NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
探究一 亚硝酸钠固体的制备
以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠。(反应方程式为2NO+Na2O2=2NaNO2,部分夹持装置和A中加热装置已略)

(1)写出装置A烧瓶中发生反应的化学方程式 。
(2)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为排除干扰应在B、C装置间增加装置E,E中盛放的试剂应是 (填字母)。
A.浓H2SO4 B.碱石灰 C.无水CaCl2
探究二 亚硝酸钠固体含量的测定及性质验证
称取装置C中反应后的固体4.000g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000
mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
|
滴定次数 |
1 |
2 |
3 |
4 |
|
KMnO4溶液体积/mL |
20.60 |
20.02 |
20.00 |
19.98 |
(3)第一组实验数据出现异常,造成这种异常的原因可能是 (填字母)。
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定终了仰视读数
(4)根据表中数据,计算所得固体中亚硝酸钠的质量分数 。
(5)亚硝酸钠易溶于水,将0.2mol·L-1的亚硝酸钠溶液和0.1mol·L-1的盐酸等体积混合,混合后溶液呈酸性,则混合后溶液中离子浓度由大到小的顺序为 。
探究三 反应废液的处理
反应后烧瓶A中仍然存在一定量的硝酸,不能直接排放,用NaOH溶液调成中性,再用电化学降解法进行处理。25℃时,反应进行10min,溶液的pH由7变为12。电化学降解NO3-的原理如右图所示。
(6)电源正极为 (填A或B),阴极反应式为 。


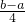
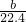 mol.L-1.
mol.L-1.

 mol.L-1.
mol.L-1.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com