
题目列表(包括答案和解析)
(5分)10℃时加热NaHCO3的饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
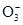 的水解程度增大,故碱性增强。
的水解程度增大,故碱性增强。(5分)10℃时加热NaHCO3的饱和溶液,测得该溶液的pH发生如下变化:
|
温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
|
pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为,该溶液的pH升高的原因是HC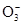 的水解程度增大,故碱性增强。
的水解程度增大,故碱性增强。
(1)乙同学认为溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于NaHCO3,该分解反应的化学方程式__________________________________。
(2)丙同学认为甲、乙的判断都不充分。丙认为:只要在加热煮沸的溶液中加入足量的BaCl2溶液,若产生沉淀,则乙判断正确。请写出该过程的离子方程式_____________;上述丙同学的实验__________(填“能”或“不能”)用Ba(OH)2溶液代替BaCl2溶液。
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
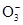 的水解程度增大,故碱性增强。
的水解程度增大,故碱性增强。(8分)10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
甲同学认为,该溶液的pH值升高的原因是HCO3—的水解程度增大,故碱性增强,该反应的离子方程式为 。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”)NaHCO3。
丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则乙判断正确。试剂X是 。A、Ba(OH)2溶液 B、NaOH溶液 C、BaCl2溶液 D、澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH (填“高于”、“低于”或“等于”)8.3,则甲判断正确。
(8分)10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
 。
。 则乙判断正确。试剂X是 。A、Ba(OH)2溶液 B、NaOH溶液 C、BaCl2溶液 D、澄清石灰水
则乙判断正确。试剂X是 。A、Ba(OH)2溶液 B、NaOH溶液 C、BaCl2溶液 D、澄清石灰水湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com