
题目列表(包括答案和解析)
联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:
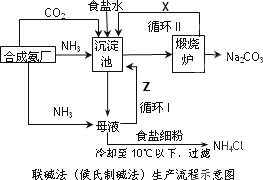
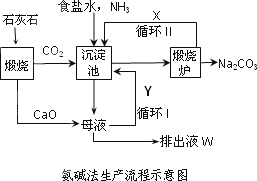
(1)沉淀池中发生反应的化学方程式为________;
(2)X是________,Y是________(填化学式);
(3)从理论上分析,在氨碱法生产过程中________(填“需要”、“不需要”)补充氨气,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为________;
(4)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是________;
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高Na+的浓度,
促进碳酸氢钠结晶析出
(5)相比于氨碱法,指出联碱法的一项优点________.
联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:
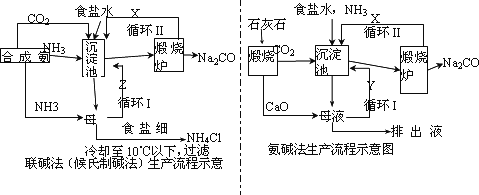
(1)沉淀池中发生反应的化学方程式为________;
(2)X是________,Y是________(填化学式);
(3)从理论上分析,在氨碱法生产过程中________(填“需要”、“不需要”)补充氨气,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为________;
(4)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是________;
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
(5)相比于氨碱法,指出联碱法的一项优点________.
联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:


(1)沉淀池中发生反应的化学方程式为________;
(2)X是________,Y是________(填化学式);
(3)从理论上分析,在氨碱法生产过程中________(填“需要”、“不需要”)补充氨气,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为________;
(4)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是________;
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
(5)相比于氨碱法,指出联碱法的一项优点________.
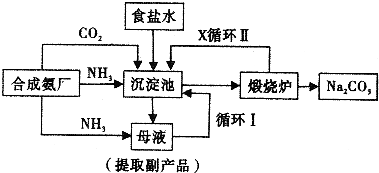
纯碱是一种重要的化工原料.目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺.请按要求回答下列问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式________.
(2)写出“联合制碱法”有关反应的化学方程式________;________.
(3)CO2是制碱工业的重要原料,“联合制碱法”和“氨碱法”中CO2的来源有何不同?
________________.
(4)绿色化学的重要原则之一是提高反应的原子利用率.根据联合制碱法的总反应,列出计算原子利用率的表达式:原子利用率(%)=________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com