
题目列表(包括答案和解析)
| ||
| ||
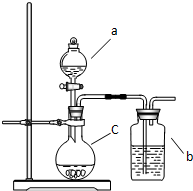 (2009?平谷区一模)在春节时,小岳同学从波力海苔包装袋内发现有一包白色颗粒状固体A的小纸袋,上面写着“生石灰干燥剂,请勿食用”.她随手将小纸袋放在写字台上,数天后发现纸袋内的白色颗粒粘在一起成为块状固体B.请你和小岳同学一起对块状固体B进行探究.
(2009?平谷区一模)在春节时,小岳同学从波力海苔包装袋内发现有一包白色颗粒状固体A的小纸袋,上面写着“生石灰干燥剂,请勿食用”.她随手将小纸袋放在写字台上,数天后发现纸袋内的白色颗粒粘在一起成为块状固体B.请你和小岳同学一起对块状固体B进行探究.| 步 骤 | 现 象 | 结 论 |
打开a仪器的活塞加入少量水,后关闭活塞. |
b中有气泡冒出,澄清石灰水不变浑浊. |
块状固体B 中含有氧化钙 中含有氧化钙 |
| 步 骤 | 现 象 | 结 论 |
向试管中滴加 酚酞试液 酚酞试液 . |
溶液变红. |
块状固体B中含有氢氧化钙. |
| 步 骤 | 现 象 | 结 论 |
| 打开a仪器的活塞,滴入适量试剂后关闭活塞. | C中有气泡生成,b中澄清的石灰水变浑浊 C中有气泡生成,b中澄清的石灰水变浑浊 . |
剩余固体中含有碳酸钙. |
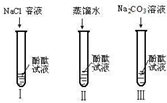 19、某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液可以使酚酞试液变红,是因为碱在水中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞试液变红呢?他们设计了如图三个实验,请你和他们一起探究并完成下列问题:
19、某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液可以使酚酞试液变红,是因为碱在水中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞试液变红呢?他们设计了如图三个实验,请你和他们一起探究并完成下列问题: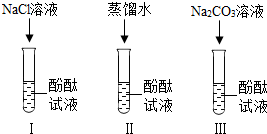 (2013?长沙)小宁和小明同学学习完酸、碱、盐后发现:碱溶液能使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液使酚酞试液变红,是因为碱在水中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?小宁设计了如图三个实验,请你、小宁和小明一起探究并完成下列问题:
(2013?长沙)小宁和小明同学学习完酸、碱、盐后发现:碱溶液能使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液使酚酞试液变红,是因为碱在水中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?小宁设计了如图三个实验,请你、小宁和小明一起探究并完成下列问题: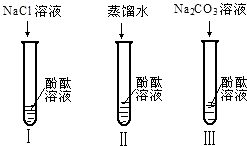 化学兴趣小组对实验室的某废液的成分进行探究,老师告诉他们废液中可能含有:NaOH、Na2CO3、CuSO4中的一种或几种.为确定废液的组成,该小组同学做了如下探究:
化学兴趣小组对实验室的某废液的成分进行探究,老师告诉他们废液中可能含有:NaOH、Na2CO3、CuSO4中的一种或几种.为确定废液的组成,该小组同学做了如下探究:湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com