
题目列表(包括答案和解析)
某校学生小组为探究乙酸、碳酸和苯酚的酸性强弱并证明乙酸为弱酸,进行下述实验。
I.探究乙酸、碳酸和苯酚的酸性强弱关系。
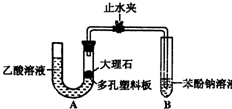
该校学生设计了如下实验装置(夹持仪器已略去)。
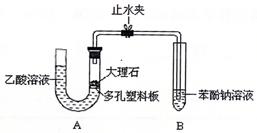
(1)实验前如何检查装置A的气密性? 。
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为________________,反应的离子方程式为 。
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,原因是 ,改进该装置的方法是 。
II.证明乙酸为弱酸。
(4)现有pH=3的乙酸溶液、蒸馏水、石蕊试液及pH试纸,用最简便的实验方法证明乙酸为弱酸。 。

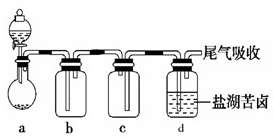 某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现在足量的稀氯化亚铁溶液中加入1~2滴溴水,振荡后溶液呈黄色.
某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现在足量的稀氯化亚铁溶液中加入1~2滴溴水,振荡后溶液呈黄色.| 编号 | 选用试剂 | 实验现象 |
| 方案1 | ||
| 方案2 |
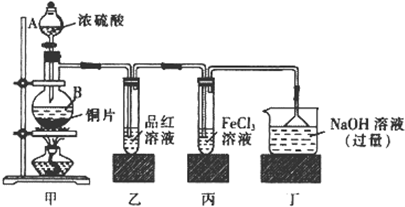
| 装置编号 | 实验现象 | 反应的离子方程式 | SO2表现的化学性质 |
| 乙 | - | ||
| 丙 | 黄色溶液变为浅绿色 |
2- 3 |
2- 4 |
2- 3 |
2- 4 |
| 编号 | 实验操作 | 预期现象和结论 | ||
| 步骤① | 取少量待测液于试管A中,滴加2mol?L-1盐酸至溶液呈酸性,加入几滴 |
| ||
| 步骤② | ||||
| 步骤③ | 另取少量待测液于试管C中,加入足量氯水,再加入四氯化碳,振荡,静置后观察颜色 | 证明待测液中含有Br- |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com