
题目列表(包括答案和解析)
题目
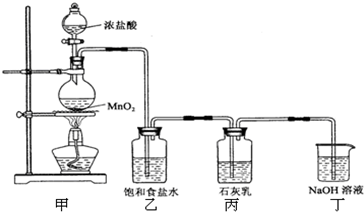
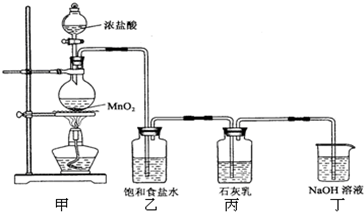
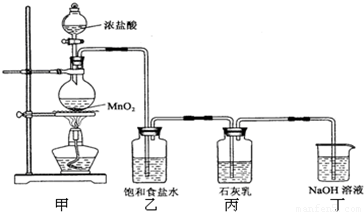
(8分)氯气与石灰乳反应可制得漂白粉,氯气在工业上可以由电解饱和食盐水来制备,产生氯气的同时,还得到氢气和氢氧化钠,称为“氯碱工业”。请回答下列问题:
(1)请写出电解饱和食盐水的化学方程式。
(2)若电解饱和食盐水时消耗氯化钠234g,试计算理论上最多可得到氯气(标准状况下)的体积为多少?
(3)若用上述制得的氯气制取漂白粉,理论上最多能得到漂白粉多少克?
| ||
| ||
| ||
| ||
| ||
 5CaCl2+Ca(ClO3)2+6H2O
5CaCl2+Ca(ClO3)2+6H2O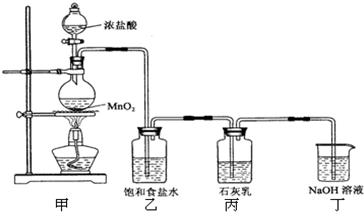
| ||
 5CaCl2+Ca(ClO3)2+6H2O
5CaCl2+Ca(ClO3)2+6H2O湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com