
题目列表(包括答案和解析)
| A、分子的稳定性:HF>H2O>NH3 | B、熔点:金刚石>汞>硫 | C、离子的半径:Cl->Al3+>Na+ | D、沸点:AsH3>PH3>NH3 |
工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是(?? )
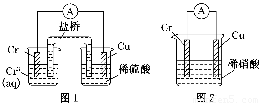
A.图1为原电池装置,Cu电极上产生的是O2
B.图2装置中Cu电极上发生的电极反应式为:Cu-2e-=Cu2+
C.由实验现象可知:金属活动性Cu>Cr
D.两个装置中,电子均由Cr电极流向Cu电极
工业上常将铬镀在其他金属表面,同铁.镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,
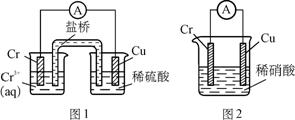
铬电极上产生大量有色气体,则下列叙述正确的是 ( )
A. 图1为原电池装置,Cu电极上产生的是O2
B. 图2装置中Cu电极上发生的电极反应式为:Cu-2e-===Cu2+
C. 由实验现象可知:金属活动性Cu>Cr
D. 两个装置中,电子均由Cr电极流向Cu电极
(1)该小组同学用该装置进行“乙炔的制取及其燃烧性质的验证”实验。①仪器a的名称是___________,实验开始时使用该仪器的操作方法是____________________________;
②点燃乙炔前,需要验纯。简述验纯的操作方法:__________________________________;
③在导管口c处点燃乙炔,观察到的现象是________________________________________。
(2)该装置还可用于制取并收集少量其他气体。请帮助该小组同学完成下表。
制取的气体 | 药品 | 化学方程式 |
O2 | __________、___________ | _____________ |
__________ | NaOH溶液、Al | ___________ |
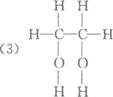
(3)某同学用该装置进行实验,确定某饱和醇的结构。反应前,先对量气管进行第一次读数;反应后,待装置温度冷却到室温,再对量气管进行第二次读数(表中读数已折合成标准状况下的数值)。实验数据记录如下:
| 饱和醇的质量 | 金属钠的质量 | 量气管第一次读数 | 量气管第二次读数 |
① | 40mL | 26mL | ||
② | 2.5(足量) | 40mL | 152mL |
已知该饱和醇的相对分子质量为62。根据上述数据可确定该饱和醇的结构式为___________。
(12分)实验室制取Cl2及性质的验证实验组合装置如下: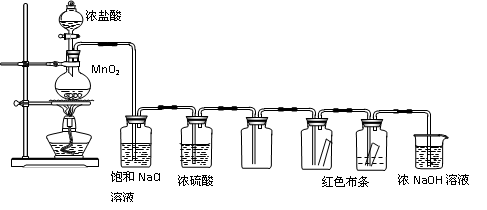
A B C D E F G
回答下列问题:
(1)A中的化学方程式为 。
(2)B的作用是除去HCl气体,C的作用是 。
(3)E、F中观察到的现象分别是 ,你得到的结论是 。
(4)G的作用是 ,
化学方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com