
题目列表(包括答案和解析)
下列物质的变化过程中,化学键没有被破坏的是( )
A.食盐溶解 B.干冰升华 C.氯化铵受热 D.电解水
【解析】食盐溶于水电离出阴阳离子,破坏了离子键。干冰升华破坏的是分子间作用力。氯化铵受热分解生成氨气和氯化氢,破坏的是化学键。电解水生成氢气和氧气,破坏的水极性键。所以答案是B。
一定条件下,下列不能用勒夏特列原理解释的是
A.工业生产硫酸的过程中使用适当过量氧气,以提高SO2的转化率
B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后气体颜色变深
C.实验室用排饱和NaHCO3溶液的方法收集CO2气体
D.新制氯水中,滴加硝酸银溶液,溶液颜色变浅,产生白色沉淀
【解析】A中增大氧气的浓度,平衡向正反应方向移动,提高SO2的转化率。氢气和碘蒸汽生成碘化氢的反应是体积不变的可逆反应,增大压强,浓度变大,颜色加深,但平衡不移动,不能用勒夏特列原理解释。C属于溶解平衡,正确。D属于沉淀溶解平衡,正确,所以答案是B。
向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入150mL4 mol·L-1的稀硝酸恰好使混合物完全溶解,放出2.24LNO(标准状况),往所得溶液中加入KSCN溶液,无红色出现。若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为:
A.0.21mol B.0.25mol C.0.3mol D.0.35mol
【解析】往所得溶液中加入KSCN溶液,无红色出现,说明所得溶液是硝酸亚铁。根据N原子守恒可知硝酸亚铁中的N原子是0.15L×4mol/L-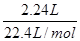 =0.5mol,所以硝酸亚铁的物质的量是0.25mol。再根据铁原子守恒可知铁的物质的量是0.25mol,所以正确的答案是B。
=0.5mol,所以硝酸亚铁的物质的量是0.25mol。再根据铁原子守恒可知铁的物质的量是0.25mol,所以正确的答案是B。
向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入150mL4 mol·L-1的稀硝酸恰好使混合物完全溶解,放出2.24LNO(标准状况),往所得溶液中加入KSCN溶液,无红色出现。若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为:
A.0.21mol B.0.25mol C.0.3mol D.0.35mol
【解析】往所得溶液中加入KSCN溶液,无红色出现,说明所得溶液是硝酸亚铁。根据N原子守恒可知硝酸亚铁中的N原子是0.15L×4mol/L-![]() =0.5mol,所以硝酸亚铁的物质的量是0.25mol。再根据铁原子守恒可知铁的物质的量是0.25mol,所以正确的答案是B。
=0.5mol,所以硝酸亚铁的物质的量是0.25mol。再根据铁原子守恒可知铁的物质的量是0.25mol,所以正确的答案是B。
下列物质的变化过程中,化学键没有被破坏的是( )
A.食盐溶解 B.干冰升华 C.氯化铵受热 D.电解水
【解析】食盐溶于水电离出阴阳离子,破坏了离子键。干冰升华破坏的是分子间作用力。氯化铵受热分解生成氨气和氯化氢,破坏的是化学键。电解水生成氢气和氧气,破坏的水极性键。所以答案是B。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com