
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
(±æ–°Ã‚15∑÷) A°¢B°¢C°¢DÀƒ‘™Àÿµƒ∫ÀµÁ∫… ˝“¿¥Œ‘ˆº”£¨À¸√«µƒ¿Î◊”µƒµÁ◊”≤„ ˝œýÕ¨«“◊ÓÕ‚≤„µÁ◊” ˝æ˘Œ™8°£A‘≠◊”µƒL≤„µÁ◊” ˝”ÎK°¢M≤„µÁ◊” ˝÷Æ∫Õœýµ»£¨D‘≠◊”µƒK°¢L≤„µÁ◊” ˝÷Æ∫Õµ»”⁄µÁ◊”◊Ð ˝µƒ“ª∞࣪ÿ¥“‘œ¬Œ £∫
°°°°(1)Àƒ‘™Àÿµƒ∑˚∫≈“¿¥Œ «A______£ªB______£ªC________£ªD______°£
°°°°(2)–¥≥ˆB°¢D‘™Àÿµƒ¿Î◊”Ω·ππ æ“‚Õº£∫
°°°°B£Æ______________________£ª D£Æ______________________°£
(3)”√µÁ◊” Ω±Ì æA°¢C‘™Àÿ–Œ≥…µƒ¿Î◊”ªØ∫œŒÔµƒπ˝≥ã∫
________________________________________________________°£
(4)‘⁄A°¢B°¢C°¢D◊Ó∏þº€—ıªØŒÔÀƪ،Ô÷–£∫
±»Ωœ∆‰÷–À·µƒÀ·–‘«ø»ı£∫____________________________£ª
±»Ωœ∆‰÷–ºÓµƒºÓ–‘«ø»ı£∫____________________________°£
(±æ–°Ã‚15∑÷) A°¢B°¢C°¢DÀƒ‘™Àÿµƒ∫ÀµÁ∫… ˝“¿¥Œ‘ˆº”£¨À¸√«µƒ¿Î◊”µƒµÁ◊”≤„ ˝œýÕ¨«“◊ÓÕ‚≤„µÁ◊” ˝æ˘Œ™8°£A‘≠◊”µƒL≤„µÁ◊” ˝”ÎK°¢M≤„µÁ◊” ˝÷Æ∫Õœýµ»£¨D‘≠◊”µƒK°¢L≤„µÁ◊” ˝÷Æ∫Õµ»”⁄µÁ◊”◊Ð ˝µƒ“ª∞࣪ÿ¥“‘œ¬Œ £∫
(1)Àƒ‘™Àÿµƒ∑˚∫≈“¿¥Œ «A______£ªB______£ªC________£ªD______°£
(2)–¥≥ˆB°¢D‘™Àÿµƒ¿Î◊”Ω·ππ æ“‚Õº£∫°°°°B£Æ______________________£ª D£Æ______________________°£
(3)”√µÁ◊” Ω±Ì æA°¢C‘™Àÿ–Œ≥…µƒ¿Î◊”ªØ∫œŒÔµƒπ˝≥ã∫ ________________________________°£
(4)‘⁄A°¢B°¢C°¢D◊Ó∏þº€—ıªØŒÔÀƪ،Ô÷–£∫
±»Ωœ∆‰÷–À·µƒÀ·–‘«ø»ı£∫____________________________£ª
±»Ωœ∆‰÷–ºÓµƒºÓ–‘«ø»ı£∫____________________________°£
(±æ–°Ã‚15∑÷) A°¢B°¢C°¢DÀƒ÷÷‘™Àÿ‘≠◊”∫ÀµÁ∫… ˝“¿¥Œ‘ˆ¥Û£®æ˘–°”⁄20£©£¨∆‰µ•÷ º∞œý”¶µƒªØ∫œŒÔƒÐ∑¢…˙»Áœ¬∑¥”¶πÿœµ£∫
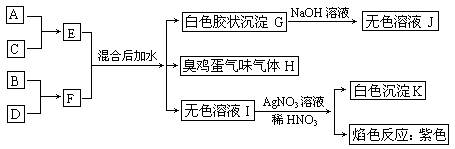
(1)–¥≥ˆÀƒ÷÷‘™Àÿ‘™Àÿ∑˚∫≈£∫A°¢____B°¢____C°¢____D°¢____°£
(2) FµƒµÁ◊” Ω£∫_________________°£
(3)–¥≥ˆE°¢FªÏ∫œ∫Ûº”ÀƵƒªØ—ß∑Ω≥Ã Ω£∫_________________________________°£
(4)–¥≥ˆGJµƒªØ—ß∑Ω≥Ã Ω£∫_________________________________°£
(5)–¥≥ˆCµ•÷ ”ÎHÀƻГ∫∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫_____________________________°£
(15∑÷)
œ÷”–∆þ÷÷‘™Àÿ£¨∆‰÷–A°¢B°¢C°¢D°¢EŒ™∂Ã÷Ð∆⁄÷˜◊‘™Àÿ£¨F°¢GŒ™µ⁄Àƒ÷Ð∆⁄‘™Àÿ£¨À¸√«µƒ‘≠◊”–Ú ˝“¿¥Œ‘ˆ¥Û°£«Î∏˘æ𜬡–œýπÿ–≈œ¢£¨ªÿ¥Œ £Æ
| A‘™Àÿµƒ∫ÀÕ‚µÁ◊” ˝∫ÕµÁ◊”≤„ ˝œýµ»£¨“≤ «”Ó÷Ê÷–◊Ó∑·∏ªµƒ‘™Àÿ |
| B‘™Àÿ‘≠◊”µƒ∫ÀÕ‚pµÁ◊” ˝±»sµÁ◊” ˝…Ÿ1 |
| C‘≠◊”µƒµ⁄“ª÷¡µ⁄ÀƒµÁ¿ÎƒÐ∑÷± «: I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D‘≠◊”∫ÀÕ‚À˘”–pπϵ¿»´¬˙ªÚ∞ά˙ |
| E‘™Àÿµƒ÷˜◊Â–Ú ˝”Î÷Ð∆⁄ ˝µƒ≤ÓŒ™4 |
| F ««∞Àƒ÷Ð∆⁄÷–µÁ∏∫–‘◊Ó–°µƒ‘™Àÿ |
| G‘⁄÷Ð∆⁄±Ìµƒµ⁄∆þ¡– |
¢≈“—÷™BA5 Œ™¿Î◊”ªØ∫œŒÔ£¨–¥≥ˆ∆‰µÁ◊” Ω £Æ
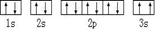
¢∆Bª˘Ã¨‘≠◊”÷–ƒÐ¡ø◊Ó∏þµƒµÁ◊”£¨∆‰µÁ◊”‘∆‘⁄ø’º‰”– ∏ˆ∑ΩœÚ£¨‘≠◊”πϵ¿≥ –Œ
 ¢«ƒ≥Õ¨—ß∏˘æð…œ ˆ–≈œ¢£¨Õ∆∂œCª˘Ã¨‘≠◊”µƒ∫ÀÕ‚µÁ◊”≈≈≤ºŒ™£∫
¢«ƒ≥Õ¨—ß∏˘æð…œ ˆ–≈œ¢£¨Õ∆∂œCª˘Ã¨‘≠◊”µƒ∫ÀÕ‚µÁ◊”≈≈≤ºŒ™£∫
∏√Õ¨—ßÀ˘ª≠µƒµÁ◊”≈≈≤ºÕºŒ•±≥¡À £Æ
¢»GŒª”⁄ ◊ «¯£¨º€µÁ◊”≈≈≤º ΩŒ™ £Æ
¢…DE3 ÷––ƒ‘≠◊”µƒ‘”ªØ∑Ω ΩŒ™ £¨”√º€≤„µÁ◊”∂‘ª•≥‚¿Ì¬€Õ∆≤‚∆‰ø’º‰ππ–Õ
Œ™ £Æ
¢ ºÏ—ÈF‘™Àÿµƒ∑Ω∑® « £¨«Î”√‘≠◊”Ω·ππµƒ÷™ ∂Ω‚ Õ≤˙…˙¥Àœ÷œÛµƒ‘≠“Ú « £Æ
¢À»Ùƒ≥µ•÷ æßÃÂ÷–‘≠◊”µƒ∂—ª˝∑Ω Ω»Áœ¬Õºº◊À˘ 棨∆‰æß∞˚Ãÿ’˜»Áœ¬Õº““À˘ 棨‘≠◊”÷ƺ‰œýª•Œª÷√πÿœµµƒ∆Ω√ÊÕº»Áœ¬Õº±˚À˘ æ°£‘Úæß∞˚÷–∏√‘≠◊”µƒ≈‰Œª ˝Œ™ £¨∏√µ•÷ æßÃÂ÷–‘≠◊”µƒ∂—ª˝∑Ω ΩŒ™Àƒ÷÷ª˘±æƒ£ Ω÷–µƒ £Æ
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com