
题目列表(包括答案和解析)
(NH4)2PtCl6晶体受热分解,生成氮气、氯化氢、氯化铵和金属铂,在此分解反应中,氧化产物与还原产物的物质的量之比是
A.2:3 B.3:2 C.4:3 D.1:3
【解析】根据反应前后的元素的化合价变化可判断,N元素由-3价升高到0,即氮气是氧化产物,每生成1mol氮气转移6mol电子。Pt的化合价由+4价降低到0价,所以Pt是还原产物。根据得失电子守恒可知生成铂的物质的量是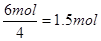 ,所以氧化产物和还原产物的物质的量之比是2:3,选项A正确。答案选A。
,所以氧化产物和还原产物的物质的量之比是2:3,选项A正确。答案选A。
已知448℃时反应H2(g)+I2(g) 2HI(g)的平衡常数是49,则
2HI(g)的平衡常数是49,则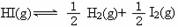 ,在该温度下的平衡常数是
,在该温度下的平衡常数是
A.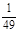 B.2401 C.7
D.
B.2401 C.7
D.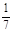
【解析】逆反应的平衡常数是正反应的倒数,H2(g)+I2(g) 2HI(g)的平衡常数是49,则1/2H2(g)+1/2I2(g)
2HI(g)的平衡常数是49,则1/2H2(g)+1/2I2(g) HI(g)的平衡常数是7,所以反应
HI(g)的平衡常数是7,所以反应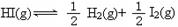 的平衡常数是1.7,答案是D。
的平衡常数是1.7,答案是D。
为了制取碘,可通过反应:2NO+O2==2NO2 NO2+2H+ +2I- ==NO + I2+H2O制得,NO在制碘过程中的作用是
A.还原剂 B.氧化剂 C.催化剂 D.反应物
【解析】根据反应观察可知反应前后NO的的量并没有发生变化,但参与了化学反应,所以起催化剂作用,答案是C。
可以充分说明反应P(g)+Q(g)⇋ R(g)+S(g)在恒温下已达到平衡的是 ( )
A、反应容器内的压强不随时间改变
B、反应容器内P、Q、R、S四者共存
C、P的生成速率和S的生成速率相等
D、反应容器内的气体总物质的量不随时间变化
【解析】因为反应前后气体的体积不变,所以气体的总物质的量就始终不变,同样压强也就始终不变,所以A、D不能说明。可逆反应的特点就是反应物和生成物同时存在,B不一定能说明。选项C中的反应速率方向相反,且满足速率之比是相应的化学计量数之比,所以可以说明已经达到平衡状态。答案是C。
最近,科学家用一种称为“超酸”的化合物H(CB11H6Cl6)和C60反应,使C60获得一个质子,得到一种新型离子化合物[HC60]+[CB11H6Cl6]-。该反应看起来很陌生,其实在反应类型上可以跟中学化学里某个熟悉的化学反应相类似。该化学反应是:
A.H2O+CH3COOH H3O++CH3COO-
B.Zn+2HCl = ZnCl2+H2↑
C.CO2+2NH3 = CO(NH2)2+H2O
D.NH3+HCl = NH4Cl
【解析】根据反应的特点可以判断类似于氯化铵的生成,因为氨气获得1个质子生成NH4+,NH4+和氯离子结合生成氯化铵,所以答案是D。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com