
题目列表(包括答案和解析)
将浓度为0.1mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是
A. 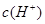 B.
B.
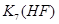 C.
C.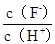 D.
D. 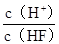
将浓度为0.1mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是
A. c(H+) B. ![]() C.
C. ![]() D.
D.![]()
下列叙述正确的是( )
A.Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制Mg
B.Al2(SO4)3可除去酸性废水中的悬浮颗粒
C将浓度为0.1mol·L-1HF 溶液加水不断稀释过程中,电离度(α)和Ka(HF)保持不变, c(F-) / c(H+)始终保持增大
D.相同数目的H318O+和D2O中子数相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com